Câu hỏi trắc nghiệm Hóa 8 Bài 36: Nước có đáp án và lời giải chi tiết
Nội dung bộ 19 bài tập trắc nghiệm Hóa 8 Bài 36: Nước được chúng tôi sưu tầm và tổng hợp kèm đáp án và lời giải được trình bày rõ ràng và chi tiết. Mời các em học sinh và quý thầy cô tham khảo dưới đây.
Bộ 19 bài tập trắc nghiệm: Nước có đáp án và lời giải chi tiết
Câu 1: Nước được cấu tạo từ các nguyên tố hóa học nào?
A. Từ 1 nguyên tử hiđro và 1 nguyên tử oxi
B. Từ 2 nguyên tử hiđro và 1 nguyên tử oxi
C. Từ 1 nguyên tử hiđro và 2 nguyên tử oxi
D. Từ 2 nguyên tử hiđro và 2 nguyên tử oxi
Lời giải:
Công thức hóa học của nước là: H2O
=> Nước được cấu tạo từ 2 nguyên tử hiđro và 1 nguyên tử oxi
Đáp án cần chọn là: B
Câu 2: Hiđro và oxi đã hóa hợp theo tỉ lệ thế nào về thể tích để tạo thành nước?
A. 2 phần khí H2 và 1 phần khí O2
B. 3 phần khí H2 và 1 phần khí O2
C. 1 phần khí H2 và 2 phần khí O2
D. 1 phần khí H2 và 3 phần khí O2
Lời giải:
Hiđro và oxi đã hóa hợp theo tỉ lệ 2 phần khí H2 và 1 phần khí O2 về thể tích để tạo thành nước
Đáp án cần chọn là: A
Câu 3: Dãy gồm các kim loại tác dụng với nước ở nhiệt độ thường là
A. Fe, Mg, Al.
B. Fe, Cu, Ag.
C. Zn, Al, Ag.
D. Na, K, Ca.
Lời giải:
Dãy gồm các kim loại tác dụng với nước ở nhiệt độ thường là: Na, K, Ca.
Đáp án cần chọn là: D
Câu 4: Kim loại không tan trong nước là:
A. Na.
B. K.
C. Ca.
D. Cu.
Lời giải:
Ghi nhớ: Chỉ có các kim loại kiềm và kiềm thổ như: Li, Na, K, Ca, Ba… tan trong nước còn lại các kim loại khác không tan.
→ Cu không tan trong nước.
Đáp án cần chọn là: D
Câu 5: Trong phân tử nước có phần trăm khối lượng H là
A. 11,1%
B. 88,97%
C. 90%
D. 10%
Lời giải:
Phần trăm khối lượng của H trong H2O là:
%mH = 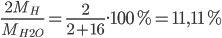
Đáp án cần chọn là: A
Câu 6: Chọn câu đúng:
A. Tất cả kim loại tác dụng với nước đều tạo ra bazơ tương ứng và khí hiđro.
B. Nước là chất lỏng không màu, không mùi, không vị.
C. Nước làm đổi màu quỳ tím.
D. Na tác dụng với H2O sinh ra khí O2.
Lời giải:
Câu đúng là: Nước là chất lỏng không màu, không mùi, không vị.
A sai vì không phải kim loại nào cũng tác dụng với nước.
C sai, nước không làm đổi màu quỳ
D sai vì Na tác dụng với H2O sinh ra khí H2.
Đáp án cần chọn là: B
Câu 7: Cho quỳ tím vào nước vôi trong, hiện tượng xảy ra là
A. Quỳ tím chuyển màu đỏ
B. Quỳ tím không đổi màu
C. Quỳ tím chuyển màu xanh
D. Không có hiện tượng
Lời giải:
Nước vôi trong là dung dịch Ca(OH)2: dung dịch bazơ => làm quỳ chuyển xanh
Đáp án cần chọn là: C
Câu 8: Oxit bazơ không tác dụng với nước là:
A. BaO
B. Na2O
C. CaO
D. MgO
Lời giải:
+ Nước có thể tác dụng với một số oxit bazơ như K2O, Na2O, CaO, BaO tạo ra bazơ
=> Oxit bazơ không tác dụng với nước là: MgO
Đáp án cần chọn là: D
Câu 9: Cho chất oxit A được nước hóa hợp tạo axit nitric. Xác định A, biết MA = 108 (g/mol), trong A có 2 nguyên tử Nitơ
A. NO2
B. N2O3
C. N2O
D. N2O5
Lời giải:
Trong A có 2 nguyên tử nitơ => gọi công thức của A có dạng N2On
Theo đầu bài: MA = 108 g/mol => 14.2 + 16.n = 108 => n = 5
Vậy công thức hóa học của A là: N2O5
Đáp án cần chọn là: D
Câu 10: Khi cho quỳ tím vào dung dịch axit, quỳ tím chuyển màu gì?
A. Đỏ
B. Xanh
C. Tím
D. Không màu
Lời giải:
Khi cho quỳ tím vào dung dịch axit, quỳ tím chuyển màu đỏ
Đáp án cần chọn là: A
Câu 11: Cho mẩu Na vào cốc nước dư thấy có 4,48 lít khí bay lên ở đktc. Tính khối lượng Na phản ứng
A. 9,2 gam
B. 4,6 gam
C. 2 gam
D. 9,6 gam
Lời giải:
Khí bay lên là H2
Số mol khí H2 là: nH2= 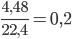 mol
mol
PTHH: 2Na + 2H2O → 2NaOH + H2
Tỉ lệ PT cứ thu được 1mol H2 thì cần dùng 2 mol Na
P/ứng: thu được 0,2mol H2 thì cần dùng: 0,2.2=0,4 mol Na
=> Khối lượng Na phản ứng là: mNa = 0,4.23 = 9,2 gam
Đáp án cần chọn là: A
Câu 12: Đốt hoàn toàn 2 mol khí H2 thì thể tích O2 cần dùng (đktc) là bao nhiêu?
A. 22,4 lít.
B. 11,2 lít.
C. 44,8 lít.
D. 8,96 lít
Lời giải:
PTHH: 2H2 + O2 → 2H2O
Tỉ lệ PT: 2mol 1mol
P/ứng: 2mol → 1 mol
=> Thể tích khí O2 cần dùng là: VO2=1.22,4=22,4 lít
Đáp án cần chọn là: A
Câu 13: Hòa tan m1 gam bari vào nước dư, thu được m2 gam Ba(OH)2 và 5,6 lít H2 (đktc). Giá trị m1 + m2 là
A. 38,5 gam.
B. 34,25 gam.
C. 42,75 gam.
D. 77 gam.
Lời giải:
Số mol khí H2 thu được là: nH2 = 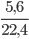 = 0,25 mol
= 0,25 mol
PTHH: Ba + 2H2O → Ba(OH)2 + H2
Tỉ lệ PT: 1mol 1mol 1mol
P/ứng: 0,25mol ← 0,25mol ← 0,25mol
=> Khối lượng Ba phản ứng là: mBa = m1 = 0,25.137 = 34,25 gam
Khối lượng Ba(OH)2 thu được là: mBa(OH)2=m2=171.0,25=42,75gam
=> Giá trị m1 + m2 = 34,25 + 42,75 = 77 gam
Đáp án cần chọn là: D
Câu 14: Cho hỗn hợp A gồm 0,92 gam Na và 8,22 gam Ba vào nước dư. Kết thúc phản ứng thu được V lít khí H2 (đktc). Giá trị của V là
A. 0,448 lít.
B. 1,344 lít.
C. 1,792 lít.
D. 2,24 lít
Lời giải:
Số mol Na là: nNa= 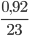 = 0,04 mol
= 0,04 mol
Số mol Ba là: nBa= 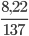 = 0,06mol
= 0,06mol
PTHH: 2Na + 2H2O → 2NaOH + H2
Tỉ lệ PT: 2mol 1mol
P/ứng: 0,04mol → 0,02mol
PTHH: Ba + 2H2O → Ba(OH)2 + H2
Tỉ lệ PT: 1 mol 1mol
P/ứng: 0,06mol → 0,06mol
=> tổng số mol H2 thu được là:
nH2=0,02+0,06=0,08mol
=> Thể tích khí H2 thu được là:
VH2=0,08.22,4=1,792 lít
Đáp án cần chọn là: C
Câu 15: Hòa tan 21,3 gam P2O5 vào nước dư, thu được m gam H3PO4. Tính m
A. 14,7.
B. 29,4.
C. 44,1.
D. 19,6.
Lời giải:
Số mol P2O5 là: nP2O5 =  = 0,15mol
= 0,15mol
PTHH: P2O5 + 3H2O → 2H3PO4
Tỉ lệ PT: 1mol 2mol
P/ứng: 0,15mol → 0,3mol
=> Khối lượng H3PO4 là: mH3PO4=0,3.98=29,4gam
Đáp án cần chọn là: B
Câu 16: Hòa tan V lít khí SO3 (đktc) gam vào nước dư, thu được 49 gam H2SO4.
Tính V
A. 11,2.
B. 22,4.
C. 16,8.
D. 19,6.
Lời giải:
Số mol H2SO4 là: nH2SO4= 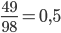 mol
mol
PTHH: SO3 + H2O → H2SO4
Tỉ lệ PT: 1mol 1mol
P/ứng: 0,5mol ← 0,5mol
=> Thể tích khí SO3 phản ứng là: VSO3 =0,5.22,4=11,2 lít
Đáp án cần chọn là: A
Câu 17: Hòa tan hỗn hợp gồm (28,4 gam P2O5 và 12 gam SO3) vào nước dư, thu được m gam hỗn hợp gồm (H3PO4 và H2SO4). Tính m
A. 39,2 gam.
B. 34,3 gam.
C. 35,9 gam.
D. 53,9 gam.
Lời giải:
Số mol P2O5 là: nP2O5= 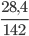 = 0,2mol
= 0,2mol
Số mol SO3 là: nSO3= 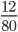 = 0,15mol
= 0,15mol
PTHH: P2O5 + 3H2O → 2H3PO4
Tỉ lệ PT: 1mol 2mol
P/ứng: 0,2mol → 0,4mol
=> Khối lượng H3PO4 là:mH3PO4=0,4.98=39,2gam
PTHH: SO3 + H2O → H2SO4
Tỉ lệ PT: 1mol 1mol
P/ứng: 0,15mol → 0,15mol
=> Khối lượng H2SO4 là: mH2SO4=0,15.98=14,7gam
=> Tổng khối lượng H3PO4 và H2SO4 thu được là: m = 39,2 + 14,7 = 53,9 gam
Đáp án cần chọn là: D
Câu 18: Hòa tan 11,28 gam K2O vào nước dư, thu được m gam KOH. Tính m
A. 6,72 gam.
B. 13,44 gam.
C. 8,4 gam.
D. 8,96 gam
Lời giải:
Số mol K2O phản ứng là:nK2O= 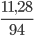 =0,12mol
=0,12mol
PTHH: K2O + H2O → 2KOH
Tỉ lệ PT: 1mol 2mol
P/ứng: 0,12mol → 0,24mol
=> Khối lượng KOH thu được là: mKOH = 0,24.56 = 13,44 gam
Đáp án cần chọn là: B
Câu 19: Hòa tan hỗn hợp gồm (12,4 gam Na2O và 15,3 gam BaO) vào nước dư, thu được m gam hỗn hợp gồm NaOH và Ba(OH)2. Tính m
A. 33,1 gam.
B. 17,1 gam.
C. 49,65 gam.
D. 26,48 gam.
Lời giải:
Số mol Na2O là: nNa2O= 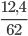 =0,2 mol
=0,2 mol
Số mol BaO là: nBaO= 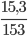 =0,1 mol
=0,1 mol
PTHH: Na2O + H2O → 2NaOH
Tỉ lệ PT: 1mol 2mol
P/ứng: 0,2mol → 0,4mol
=> Khối lượng NaOH thu được là: mNaOH = 0,4.40 = 16 gam
PTHH: BaO + H2O → Ba(OH)2
Tỉ lệ PT: 1mol 1mol
P/ứng: 0,1mol → 0,1mol
=> Khối lượng Ba :mBa(OH)2=0,1.171=17,1gam
=> Tổng khối lượng NaOH và Ba(OH)2 là:
m = 16 + 17,1 = 33,1 gam
Đáp án cần chọn là: A
►► CLICK NGAY vào nút TẢI VỀ dưới đây để tải về Bộ 19 bài tập trắc nghiệm về Nước có đáp án và lời giải chi tiết file PDF hoàn toàn miễn phí.
 Soạn Hóa 8 Bài 24: Tính chất của oxi đầy đủ nhất
Soạn Hóa 8 Bài 24: Tính chất của oxi đầy đủ nhất Giải SBT Hóa 8 Bài 2: Chất (ngắn gọn nhất)
Giải SBT Hóa 8 Bài 2: Chất (ngắn gọn nhất) [LỜI GIẢI] Phản ứng nào là phản ứng hóa hợp?
[LỜI GIẢI] Phản ứng nào là phản ứng hóa hợp? Câu hỏi trắc nghiệm Hóa 8 Bài 2: Chất có đáp án và lời giải chi tết
Câu hỏi trắc nghiệm Hóa 8 Bài 2: Chất có đáp án và lời giải chi tết Câu hỏi trắc nghiệm Hóa 8 Bài 4: Nguyên tử có đáp án và lời giải chi tiết
Câu hỏi trắc nghiệm Hóa 8 Bài 4: Nguyên tử có đáp án và lời giải chi tiết Câu hỏi trắc nghiệm Hóa 8: Cách giải bài tập về Tính phân tử khối có đáp án và lời giải chi tết
Câu hỏi trắc nghiệm Hóa 8: Cách giải bài tập về Tính phân tử khối có đáp án và lời giải chi tết Giải Hóa học 8 Bài 28: Không khí - Sự cháy (Ngắn gọn nhất)
Giải Hóa học 8 Bài 28: Không khí - Sự cháy (Ngắn gọn nhất) Câu hỏi trắc nghiệm Hóa 8: Lập công thức hóa học dựa vào thành phần nguyên tử có đáp án và lời giải chi tiết
Câu hỏi trắc nghiệm Hóa 8: Lập công thức hóa học dựa vào thành phần nguyên tử có đáp án và lời giải chi tiết

