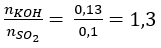Câu hỏi trắc nghiệm Hóa 10 Bài 33: Axit sunfuric - Muối sunfat có đáp án
Chúng tôi xin giới thiệu các bạn học sinh bộ tài liệu giải Bài tập trắc nghiệm Hóa học 10 Bài 33: Axit sunfuric - Muối sunfat có lời giải hay, cách trả lời ngắn gọn, đủ ý được biên soạn bởi đội ngũ chuyên gia giàu kinh nghiệm. Mời các em tham khảo tại đây.
Bộ 16 bài tập trắc nghiệm: Axit sunfuric - Muối sunfat có đáp án và lời giải chi tiết
Câu 1: Kim loại nào sau đây không tác dụng với dung dịch H2SO4 loãng?
A. Al
B. Mg
C. Na
D. Cu
Đáp án: D
Câu 2: Dãy kim loại nào trong các dãy sau đây gồm các kim loại đều không tác dụng với dung dịch H2SO4 loãng?
A. Al, Mg, Cu
B. Fe, Mg, Ag
C. Al, Fe, Mg
D. Al, Fe, Cu
Đáp án: C
Câu 3: Dãy kim loại nào trong các dãy sau đây gồm các kim loại đều không tác dụng với dung dịch H2SO4 đặc, nguội?
A. Al, Fe, Au, Mg
B. Zn, Pt, Au, Mg
C. Al, Fe, Zn, Mg
D. Al, Fe, Au, Pt
Đáp án: D
Câu 4: Cho phương trình hóa học:
aAl + bH2SO4 → cAl2(SO4)3 + dSO2 + e H2O
Tỉ lệ a:b là
A. 1:1
B. 2:3
C. 1:3
D. 1:2
Đáp án: C
Câu 5: Phương trình hóa học nào sau đây không đúng?
A. Cu + 2H2SO4 (đặc) → CuSO4 +SO2 + 2H2O
B. Fe + S to → FeS
C. 2Ag + O3 → Ag2O + O2
D. 2Fe + 3H2SO4 (loãng) → Fe2(SO4)3 + 3H2
Đáp án: D
Câu 6: Trong điều kiện thích hợp, có thể xảy ra các phản ứng sau:
H2SO4 + C → 2SO2 + CO2 + 2H2O
H2SO4 + Fe(OH)2 → FeSO4 + 2H2O
4H2SO4 +2FeO → Fe2(SO4)3 + SO2 + 4H2O
6H2SO4 + 2Fe → Fe2(SO4)3 + 3SO2 + 6H2O
Trong các phản ứng trên, khi dung dịch H2SO4 là dung dịch loãng thì phản ứng nào có thể xảy ra?
A. (a)
B. (c)
C. (b)
D. (d)
Đáp án: C
Câu 7: Cho các chất: KBr, S, SiO2, P, Na3PO4, FeO, Cu và Fe2O3. Trong các chất đã cho, số chất có thể bị oxi hóa bởi dung dịch axit H2SO4 đặc, nóng là
A. 5
B. 4
C. 6
D. 7
Đáp án: A
Câu 8: Cho hỗn hợp gồm 1 mol chất X và 1 mol chất Y tác dụng hết với dung dịch H2SO4 đăc, nóng (dư) tạo ra 1 mol khí SO2 (sản phẩm khử duy nhất). Hai chất X, Y là
A. Fe, Fe2O3
B. Fe, FeO
C. Fe3O4, Fe2O3
D. FeO, Fe3O4
Đáp án: D
Câu 9: Hòa tan hoàn toàn 5,5 gam hỗn hợp gồm Al và Fe vào lượng dư dung dịch H2SO4 loãng, thu được 4,48 lít H2 (đktc). Thành phần phần trăm khối lượng của Fe trong hỗn hợp đầu là
A. 50,91%
B. 76,36%
C. 25,45%
D. 12,73%
Đáp án: A
nH2 = 4,48/22,4 = 0,2 (mol)
⇒ mhh= mFe + mAl
Bảo toàn electron: 2nFe + 3nAl =2nH2
⇒ 56nFe + 27nAl = 5,5 ; 2nFe + 3nAl = 2.0,2
⇒ nFe = 0,05 ; nAl = 0,1 ⇒ %mFe = 0,05.56/5,5.100% = 50,91%
Câu 10: Hòa tan 12,8 gam Cu trong axit H2SO4 đặc, nóng dư. Thể tích khí SO2 thu được (đktc) là
A. 4,48 lít
B. 2,24 lít
C. 6,72 lít
D. 8,96 lít
Đáp án: A
nCu = 12,8/64 = 0,2 (mol)
Bỏa toàn electron: 2nSO2 = 2nCu
⇒ nSO2 = nCu = 0,2 (mol) ⇒ V = 0,2.22,4 = 4,48 (lít)
Câu 11: Cho m gam hỗn hợp X gồm Al, Cu vào dung dịch H2SO4 loãng (dư), thu được 6,72 lít khí (đktc). Nếu cho m gam hỗn hợp X trên vào một lượng dư dung dịch H2SO4 (đặc, nguội), thu được 6,72 lít khí SO2 (sản phẩm khử duy nhất, ở đktc). Giá trị của m là
A. 23,0
B. 21,0
C. 24,6
D. 30,2
Đáp án: C
nH2 = 6,72/22,4 = 0,3 (mol); nSO2 =6,72/22,4 = 0,3 (mol)
Bảo toàn electron:
3nAl = 2nH2 ; 2nCu = 2nSO2
⇒ nAl = 0,2; nCu = 0,3 ⇒ m = 0,2.27 + 0,3.64 = 24,6 (gam)
Câu 12: Hòa tan hoàn toàn 3,22 gam hỗn hợp X gồm Fe, Mg và Zn bằng 1 lượng vừa đủ dung dịch H2SO4 loãng, thu được 1,344 lít khí hidro (đktc) và dung dịch chứa m gam muối. Giá trị của m là
A. 9,52
B. 10,27
C. 8,98
D. 7,25
Đáp án: C
nH2 = 1,334/22,4 = 0,06 (mol) ⇒ nH2SO4 = nH2 = 0,06 mol
Bảo toàn khối lượng: 3,22 + 0,06.98 = m + 0,06.2
m = 8,98 gam
Câu 13: Cho 3,68 gam hỗn hợp gồm Al và Zn tác dụng với một lượng vừa đủ dung dịch H2SO4 10%, thu được 2,24 lít khí H2 (đktc). Khối lượng dung dịch thu được sau phản ứng là
A. 97,80 gam
B. 101,48 gam
C. 88,20 gam
D. 101,68 gam
Đáp án: B
nH2 = 2,24/22,4 = 0,1 mol ⇒ mdd H2SO4 = 0,1.98.100/10 = 98 gam
mdd sau = 3,68 + 98 – (0,1.2) = 101,48 (gam)
Câu 14: Hòa tan hoàn toàn 2,81 gam hỗn hợp gồm Fe2O3, MgO, ZnO trong 500 ml axit H2SO4 0,1M (vừa đủ). Sau phản ứng cô cạn dung dịch hỗn hợp muối sunfat khan thu được có khối lượng là
A. 6,81 gam
B. 4,81 gam
C. 3,81 gam
D. 5,81 gam
Đáp án: A
nH2O = nH2SO4 = 0,1.0,5 = 0,05 (mol)
Bảo toàn khối lượng: 2,81 + 0,05.98 = m + 0,05.18
m = 6,81 gam
Câu 15: Hòa tan hết 0,2 mol FeO bằng dung dịch H2SO4 đặc, nóng (dư), thu được khí SO2 (sản phẩm khử duy nhất). Hấp thụ hoàn toàn khí SO2 sinh ra ở trên vào dung dịch chứa 0,13 mol KOH, thu được dung dịch chứa m gam muối. Giá trị của m là
A. 15,80
B. 14,66
C. 15,60
D. 13,14
Đáp án:
Bảo toàn electron: 2nSO2 = nFeO ⇒ nSO2 = 0,1mol
nNa2SO3 = nNaOH - nSO2 = 0,13 – 0,1 = 0,03 (mol)
⇒ nNaHSO3 = 0,07 mol
⇒ m = 0,07.120 + 0,03.158 = 13,14 (gam)
Câu 16: Cho 0,015 mol một loại hợp chất oleum vào nước thu được 200ml dung dịch X. Để trung hòa 100 ml dung dịch X cần dùng 200 ml dung dịch NaOH 0,15M. Thành phần phần trăm về khối lượng của nguyên tố lưu huỳnh trong oelum trên là
A. 37,86%
B. 35,96%
C. 23,97%
D. 32,655%
Đáp án: B
nNaOH = 0,15. 0,2 = 0,03 mol ⇒ nNaOH(200ml X) = 0,06 mol
H2SO4.nSO3 (0,015) + nH2O → (n+1)H2SO4 (0,015(n + 1) mol)
H2SO4 (0,15(n+1)) + 2NaOH (0,03(n+1) mol) → Na2SO4 + 2H2O
0,03(n + 1) = 0,06 ⇒ n = 1 ⇒ oleum: H2SO4.SO3
%mS = [(2.32)/(98 + 80)]. 100% = 35,96%
►► CLICK NGAY vào nút TẢI VỀ dưới đây để download giải Bài tập trắc nghiệm Hóa học 10 Bài 33: Axit sunfuric - Muối sunfat chi tiết bản file pdf hoàn toàn miễn phí từ chúng tôi.
 [ĐÁP ÁN] Nguyên tố hóa học là tập hợp những nguyên tử có cùng?
[ĐÁP ÁN] Nguyên tố hóa học là tập hợp những nguyên tử có cùng? Giải Hoá học 10 Bài 37: Bài thực hành số 6 trang 155 SGK
Giải Hoá học 10 Bài 37: Bài thực hành số 6 trang 155 SGK [ĐÁP ÁN] Liên kết hóa học trong phân tử HCl là?
[ĐÁP ÁN] Liên kết hóa học trong phân tử HCl là? Soạn Hóa 10 Bài 21: Khái quát về nhóm Halogen đầy đủ nhất
Soạn Hóa 10 Bài 21: Khái quát về nhóm Halogen đầy đủ nhất Báo cáo bài thực hành Hóa 10 Bài 20: Phản ứng oxi hóa khử chi tiết
Báo cáo bài thực hành Hóa 10 Bài 20: Phản ứng oxi hóa khử chi tiết [ĐÁP ÁN] Trong phòng thí nghiệm, người ta thường điều chế clo bằng cách?
[ĐÁP ÁN] Trong phòng thí nghiệm, người ta thường điều chế clo bằng cách? Giải Hoá học 10 Bài 39: Luyện tập trang 166, 167 SGK
Giải Hoá học 10 Bài 39: Luyện tập trang 166, 167 SGK Giải SBT Hóa học 10 Bài 12: Liên kết ion - Tinh thể ion (chính xác nhất)
Giải SBT Hóa học 10 Bài 12: Liên kết ion - Tinh thể ion (chính xác nhất)