Soạn Hóa 10 Bài 21: Khái quát về nhóm Halogen đầy đủ nhất
Để quá trình tiếp thu kiến thức mới trở nên dễ dàng và đạt hiệu quả nhất, trước khi bắt đầu bài học mới các em cần có sự chuẩn bị nhất định qua việc tổng hợp nội dung kiến thức lý thuyết trọng tâm, sử dụng những kiến thức hiện có thử áp dụng giải các bài tập ứng dụng, trả lời câu hỏi liên quan. Dưới đây chúng tôi đã soạn sẵn Lời giải Hóa 10 Bài 21: Khái quát về nhóm Halogen đầy đủ nhất, giúp các em tiết kiệm thời gian. Nội dung chi tiết được chia sẻ dưới đây.
Bài 21: Khái quát về nhóm Halogen
Bài tập SGK
Bài 1 (trang 96 SGK Hóa 10):
Kim loại nào sau đây tác dụng với dung dịch HCl loãng và tác dụng với khí Cl2 cho cùng loại muối clorua kim loại?
A. Fe.
B. Zn.
C. Cu.
D. Ag.
Hướng dẫn giải chi tiết:
- Kim loại Zn tác dụng với dung dịch HCl loãng và với khí clo cho cùng loại muối clorua kim loại.
Zn + 2HCl → ZnCl2 + H2.
Zn + Cl2 → ZnCl2.
- Kim loại sắt tác dụng với dung dịch HCl loãng và khí clo cho 2 loại muối clorua khác nhau là FeCl2 và FeCl3.
Fe + 2HCl → FeCl2 + H2.
2Fe + 3Cl2 → 2FeCl3.
Ag, Cu không tác dụng với dung dịch HCl.
Bài 2 (trang 96 SGK Hóa 10):
Đặc điểm nào dưới đây không phải là đặc điểm chung của các nguyên tố halogen (F, Cl, Br, I)?
A. Nguyên tử chỉ có khả năng thu thêm 1e.
B. Tạo ra với hidro hợp chất có liên kết cộng hóa trị có cực.
C. Có số oxi hóa – 1 trong mọi hợp chất.
D. Lớp electron ngoài cùng của nguyên tử có 7 electron.
Hướng dẫn giải chi tiết:
C đúng.
Trong tất cả các hợp chất F chỉ có số oxi hóa -1 do F có độ âm điện lớn nhất.
Các nguyên tố halogen khác ngoài số oxi hóa -1 còn có các số oxi hóa +1; +3; +5; +7
Bài 3 (trang 96 SGK Hóa 10):
Đặc điểm nào dưới đây là đặc điểm chung của các đơn chất halogen (F2, Cl2, Br2,I2):
A. Ở điều kiện thường là chất khí.
B. Có tính oxi hóa mạnh.
C. Vừa có tính oxi hóa, vừa có tính khử.
D. Tác dụng mạnh với nước.
Hướng dẫn giải chi tiết:
B đúng.
Bài 4 (trang 96 SGK Hóa 10):
So sánh những nguyên tố halogen về các mặt sau:
a) Cấu tạo nguyên tử và cấu tạo phân tử.
b) Tính chất vật lí.
c) Tính chất hóa học.
Hướng dẫn giải chi tiết:
So sánh những nguyên tố halogen về các mặt sau:
a) Cấu tạo nguyên tử và cấu tạo phân tử:
- Giống nhau:
+ Số lớp electron ngoài cùng có 7e. Ở trạng thái cơ bản, nguyên tử halogen đều có 1 electron độc thân.
+ Phân tử 2 nguyên tử, liên kết cộng hóa trị không cực.
+ Cấu hình electron lớp ngoài cùng ns2np5.
- Khác nhau:
+ Bán kính nguyên tử tăng dần từ flo đến iot.
+ Số lớp electron tăng dần từ flo đến iot.
+ Lớp ngoài cùng của nguyên tố flo là lớp thứ 2 nên không có phân lớp d. Nguyên tử clo, brom và iot có phân lớp d còn trống.
+ Ở trạng thái kích thích, nguyên tử clo, brom hoặc iot có thể có 3, 5 hoặc electron độc thân.
+ Độ âm điện giảm dần từ flo đến iot.
b) Tính chất vật lí
Trong nhóm halogen, tính chất vật lí biến đổi có quy luật: Trạng thái tập hợp, màu sắc, nhiệt độ nóng chảy, nhiệt độ sôi ...
Từ flo đến iot ta nhận thấy:
- Trạng thái tập hợp: Từ thể khí chuyển sang thể lỏng và thể rắn.
- Màu sắc: đậm dần
- Nhiệt độ nóng chảy và nhiệt độ sôi: tăng dần.
- Flo không tan trong nước vì nó phân hủy nước rất mạnh, các halogen khác tan tương đối ít trong nước và tan nhiều trong một số dung môi hữu cơ.
c) Tính chất hóa học:
Giống nhau:
- Vì lớp electron lớp ngoài cùng có cấu tạo tương tự nhau (...ns2np5) nên các halogen rất giống nhau về tính chất hóa học của đơn chất cũng như về thành phần và tính chất của các hợp chất.
- Halogen có ái lực với electron lớn. Nguyên tử halogen X với 7 electron lớp ngoài cùng dễ dàng thu thêm 1 electron để trở thành ion âm.
X + 1e → X-
- Oxi hóa được hầu hết các kim loại tạo muối halogennua.
Khác nhau:
- Khả năng oxi hóa của các halogen giảm dần từ flo đến iot.
- Phản ứng với kim loại, với hidro, với nước của các halogen cũng có khác nhau.
- Flo không thể hiện tính khử (không có số oxi hóa dương) còn các halogen khác có tính khử và tính khử tăng dần từ flo đến iot.
Bài 5 (trang 96 SGK Hóa 10):
Hãy cho biết tính quy luật của sự biến đổi của nhiệt độ nóng chảy nhiệt độ sôi, màu sắc, độ âm điện của nguyên tố halogen.
Hướng dẫn giải chi tiết:
Quy luật của sự biến đổi tính chất vật lí và độ âm điện của các halogen là:
- Nhiệt độ nóng chảy và nhiệt độ sôi tăng dần từ flo đến iot.
- Màu sắc đậm dần từ flo đến iot.
- Độ âm điện giảm dần từ flo đến iot.
Bài 6 (trang 96 SGK Hóa 10):
Nêu tính chất hóa học cơ bản của các nguyên tố halogen. Giải thích chiều biến đổi của tính chất hóa học cơ bản đó trong nhóm.
Hướng dẫn giải chi tiết:
Tính chất hóa học cơ bản của các halogen là tính oxi hóa mạnh, các nguyên tử này rất hoạt động vì chúng dễ thu thêm 1 electron, tính oxi hóa của các halogen giảm dần từ flo đến iot. Sở dĩ tính oxi hóa giảm dần từ flo đến iot là do:
- Độ âm điện giảm dần từ flo đến iot.
- Từ flo qua clo đến brom và iot, lớp electron ngoài cùng càng xa hạt nhân hơn, bán kính nguyên tử tăng dần, lực hút của hạt nhân với electron ngoài cùng càng yếu hớn, làm cho khả năng nhận electron của halogen giảm dần.
Bài 7 (trang 96 SGK Hóa 10):
Giải thích vì sao các nguyên tố halogen không có ở trạng thái tự do trong tự nhiên.
Hướng dẫn giải chi tiết:
Các nguyên tố halogen không có ở trạng thái tự do trong thiên nhiên do nguyên tử của các nguyên tố này hoạt động này hoạt động hóa học rất mạnh.
Bài 8 (trang 96 SGK Hóa 10):
Cho một lượng đơn chất halogen tác dụng với Mg thu được 19g magie halogenua. Cũng lượng đơn chất halogen đó tác dụng với nhôm tạo 17,8g nhôm halogen. Xác định tên và khối lượng đơn chất halogen nói trên.
Hướng dẫn giải chi tiết:
a) Phương trình hóa học của phản ứng: Gọi X là kí hiệu nguyên tử khối của halogen.
Mg + X2 → MgX2
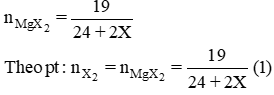
2Al + 3X2 → 2AlX3.
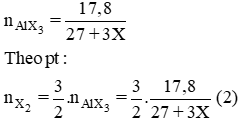
Cho (1) = (2). Giải ta rút ra X = 35,5 (Cl)
b) Thay X = 35,5 vào (1) ⇒ nCl2 = 0,2 mol ⇒ mCl2 = 14,2g.
Bộ câu hỏi trắc nghiệm
Câu 1: Những nguyên tố halogen thuộc nhóm
A. IA B. VA C. VIA D. VIIA
Đáp án: D
Câu 2: Cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố halogen là
A. ns2np4 B. ns2np5 C. ns2np3 D. ns2np6
Đáp án: B
Câu 3: Nguyên tố có độ âm điện lớn nhất là
A. clo B. brom C. flo D. iot
Đáp án: C
Câu 4: Trong nhóm halogen, sự biến đổi tính chấ nào sau đây của đơn chất đi từ flo đến iot là đúng?
A. Ở điều kiện thường, trạng thái tập hợp chuyển từ thể khí sang thể lỏng và rắn.
B. Màu sắc nhạt dần.
C. Nhiệt độ nóng chảy giảm dần.
D. Tính oxi hóa tăng dần.
Đáp án: A
Câu 5: Đặc điểm chung của các đơn chất halogen (F2, Cl2, Br2, I2) :
A. ở điều kiện thường là chất khí.
B. tác dụng mãnh liệt với nước.
C. vừa cso tính oxi hóa, vừa có tính khử.
D. tính chất hóa học cơ bản là tính oxi hóa.
Đáp án: D
Câu 6: Dung dịch muối không tác dụng với dung dịch AgNO3 là
A. NaF B. NaCl C. NaBr D. NaI
Đáp án: A
Câu 7: Phát biểu nào sau đây sai?
A. Độ âm điện của brom lớn hơn độ âm điện của iot.
B. Flo có tính oxi hóa mạnh hơn clo.
C. Trong các hợp chất, flo và clo có các số oxi hóa -1, +1, +3, +5, +7.
D. Bán kính nguyên tử của clo lớn hơn bán kính nguyên tử của flo.
Đáp án: C
Câu 8: Cho dung dịch chứa 6,03 gam hỗn hợp gồm hai muối NaX và NaY (X, Y là hai nguyên tố có trong tự nhiên, ở hai chu kì liên tiếp thuộc nhóm VIIA, số hiệu nguyên tử ZX < ZY) vào dung dịch AgNO3 (dư), thu được 8,61 gam kết tủa. Thành phần phần trăm khối lượng của NaX trong hỗn hợp ban đầu là
A. 47,2 % B. 52,8 C. 58,2% D. 41,8%
Đáp án: D
Giả sử Y không phải Flo
Gọi CTTB của X và Y là X
NaX → AgX
23 + X → 108 + X (g)
6,03 → 8,61 (g)
8,61.(23 + X) = 6,03. (108 + X)
X = 175,3 (Loại)
X là Clo, Y là Flo
Kết tủa chỉ gồm AgCl; nAgCl = nNaCl = 8,61 : 143,5 = 0,06 mol
% mNaCl = 0,06.58,5 : 6,03. 100% = 58,2% ⇒ % mNaF = 41,2%
Câu 9: Sục khí clo dư vào dung dịch chứa muối NaBr và KBr thu được muối NaCl và KCl, đồng thời thấy khối lượng muối giảm 4,45 gam. Thể tích khí clo đã tham gia phản ứng với 2 muối trên (đo ở đktc) là
A. 4,48 lít. B. 3,36 lít.
C. 2,24 lít. D. 1,12 lít.
Đáp án: D
MBr + 1/2 Cl2 → MCl + 1/2 Br2
1 mol muối giảm = 80 – 35,5 = 44,5g
⇒ nCl2 = 1/2. nmuối = 1/2 . 4,45/44,5 = 0,05 mol
⇒ VCl2 = 1,12l
Câu 10: Cho 4 đơn chất F2; Cl2; Br2; I2. Chất có nhiệt độ sôi cao nhất là :
A. F2. B. Cl2.
C. Br2. D. I2.
Đáp án: D
Câu 11: Cho các phản ứng hóa học sau, phản ứng nào chứng minh Cl2 có tính oxi hoá mạnh hơn Br2 ?
A. Br2 + 2NaCl → 2NaBr + Cl2
B. Cl2 + 2NaOH → NaCl + NaClO + H2O
C. Br2 + 2NaOH → NaBr + NaBrO + H2O
D. Cl2 + 2NaBr → 2NaCl + Br2
Đáp án: D
Câu 12: Hỗn hợp X gồm NaBr và NaI. Cho hỗn hợp X tan trong nước thu được dung dịch A. Nếu cho brom dư vào dung dịch A, sau phản ứng hoàn toàn, cô cạn thấy khối lượng muối khan thu được giảm 7,05 gam. Nếu sục khí clo dư vào dung dịch A, phản ứng hoàn toàn, cô cạn dung dịch thấy khối lượng muối khan giảm 22,625 gam. Thành phần % khối lượng của một chất trong hỗn hợp X là:
A. 64,3%. B. 39,1%.
C. 47,8%. D. 35,9%
Đáp án: C
NaBr (x mol); NaI (y mol)
Cho Br2 vào dung dịch A chỉ phản ứng với NaI
NaI + 1/2 Br2 → NaBr + 1/2 I2
1 mol NaI → 1 mol NaBr giảm 47g
⇒ nNaI = 0,15 mol = y
Khi sục khí Clo: m giảm = x.(80 – 35,5) + y (127-35,5) = 22,625g
⇒ x = 0,2 mol
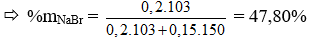
Câu 13: Hãy chỉ ra mệnh đề không chính xác:
A. Tất cả muối AgX (X là halogen) đều không tan trong nước.
B. Tất cả các hiđro halogenua đều tồn tại ở thể khí, ở điều kiện thường.
C. Tất cả các hiđro halogenua khi tan vào nước đều cho dung dịch axit.
D. Các halogen (từ F2 đến I2) tác dụng trực tiếp với hầu hết các kim loại.
Đáp án: A
Câu 14: Đốt cháy 11,9 gam hỗn hợp gồm Zn, Al trong khí Cl2 dư. Sau khi các phản ứng xảy ra hoàn toàn, thu được 40,3 gam hỗn hợp muối. Thể tích khí Cl2 (đktc) đã phản ứng là
A. 8,96 lít. B. 6,72 lít.
C. 17,92 lít. D. 11,2 lít.
Đáp án: A
Bảo toàn khối lượng: mCl2 = mmuối – mkim loại = 28,4g
⇒ VCl2 = (28,4:71). 22,4 = 8,96l
Câu 15: Trong các phản ứng hoá học, để chuyển thành anion, nguyên tử của các nguyên tố halogen đã nhận hay nhường bao nhiêu electron ?
A. Nhận thêm 1 electron.
B. Nhận thêm 2 electron.
C. Nhường đi 1 electron.
D. Nhường đi 7 electron.
Đáp án: A
Lý thuyết trọng tâm
I. Nhóm halogen trong bảng tuần hoàn các nguyên tố
- Gồm có các nguyên tố 9F 17Cl 35Br 53I 85At. Phân tử dạng X2 như F2 khí màu lục nhạt, Cl2 khí màu vàng lục, Br2 lỏng màu nâu đỏ, I2 tinh thể tím.
II. Cấu hình electron nguyên tử và cấu tạo phân tử của các nguyên tố trong nhóm halogen
- Cấu hình electron lớp ngoài cùng của nguyên tử các halogen là ns2np5
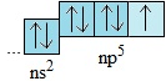
- Dễ nhận thêm một electron để đạt cấu hình bền vững của khí hiếm
X + 1e → X- (X: F, Cl, Br, I)
- Ở trạng thái cơ bản, nguyên tử các halogen đều có một electron độc thân.
- Lớp electron ngoài cùng của nguyên tử flo là lớp thứ hai nên không có phân lớp d. Nguyên tử clo, brom và iot có phân lớp d còn trống, khi được kích thích 1, 2 hoặc 3 electron có thể chuyển đến những obitan d còn trống:
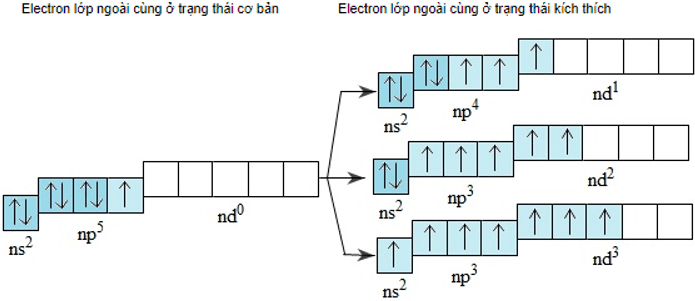
Do đó ở các trạng thái kích thích, nguyên tử clo, brom hoặc iot có thể có 3, 5 hoặc 7 electron độc thân.
III. Khái quát về tính chất của các halogen
1. Tính chất vật lý
- Nhiệt độ nóng chảy và nhiệt độ sôi: Tăng dần từ F đến I.
- Nguyên tử halogen có 7e lớp ngoài cùng ns2np5, bán kính nguyên tử nhỏ, có độ âm điện lớn ⇒ dễ nhận e, halogen có tính oxi hóa mạnh và là phi kim điển hình.
Ion halogenua X- có mức oxi hóa thấp nhất nên thể hiện tính khử.

- Giữa các phân tử X2 chỉ có lực hút Van der Waals yếu nên các halogen hoặc ở trạng thái khí (F2, Cl2) hoặc ở trạng thái lỏng (Br2) dễ bay hơi, cũng có thể ở trạng thái rắn(I2) dễ thăng hoa.
- Tính tan: Flo phân hủy nước rất mạnh nên không tan trong nước.
Các halogen khác tan tương đối ít trong nước và tan nhiều trong dung môi hữu cơ.
2. Tính chất hóa học
- Cấu hình e lớp ngoài cùng tương tự nhau nên các halogen có nhiều điểm giống nhau về tính chất hóa học:
+ Có 7 e lớp ngoài cùng nên có xu hướng nhận thêm 1 e tạo thành ion âm X-.
+ Là phi kim điển hình, có tính oxi hóa mạnh.
- Tính oxi hóa của halogen:
Nhóm halogen với 7 điên tử ở lớp ngoài cùng và độ âm điện lớn, nguyên tử halogen X dễ dàng lấy 1 điện tử tạo ra X-có cấu hình khí trơ bền vững.
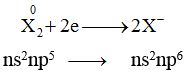
Do đó tính chất quan trọng nhất của nhóm halogen là tính oxi hóa, tính này giảm dần từ F2 (chất oxi hóa mạnh nhất) đến I2 (chất oxi hóa trung bình).
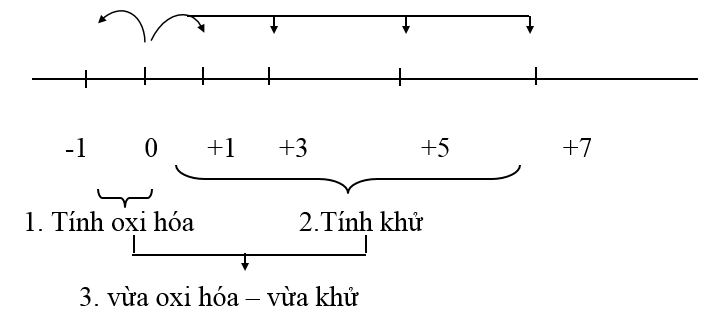
Các bậc oxi hóa đặc trưng của các halogen là: -1, 0, +1, +3, +5, +7 (trừ F luôn có số oxi hóa -1).
Ở dạng đơn chất, các halogen tồn tại dưới dạng phân tử X2. Có bậc oxi hóa trung gian là 0 là bậc oxi hóa trung gian. Nên nó vừa thể hiện tính oxi hóa vừa thể hiện tính khử.
File tải hướng dẫn soạn Hóa 10 Bài 21: Khái quát về nhóm halogen:
Hy vọng tài liệu sẽ hữu ích cho các em học sinh và quý thầy cô giáo tham khảo..
►Ngoài ra các em học sinh và thầy cô có thể tham khảo thêm nhiều tài liệu hữu ích hỗ trợ ôn luyện thi môn hóa như đề kiểm tra học kì, 1 tiết, 15 phút trên lớp, hướng dẫn giải sách giáo khoa, sách bài tập được cập nhật liên tục tại chuyên trang của chúng tôi.
 Soạn Hóa 10 Bài 21: Khái quát về nhóm Halogen đầy đủ nhất
Soạn Hóa 10 Bài 21: Khái quát về nhóm Halogen đầy đủ nhất Soạn Hóa học 10 Bài 22: Clo chi tiết nhất
Soạn Hóa học 10 Bài 22: Clo chi tiết nhất Giải Hoá học 10 Bài 28: Bài thực hành số 3 trang 120 SGK
Giải Hoá học 10 Bài 28: Bài thực hành số 3 trang 120 SGK Giải Hoá học 10 Bài 26: Luyện tập nhóm halogen trang 118 - 119 SGK
Giải Hoá học 10 Bài 26: Luyện tập nhóm halogen trang 118 - 119 SGK Giải Hoá học 10 Bài 25: Flo - Brom - Iot trang 113 - 114 SGK
Giải Hoá học 10 Bài 25: Flo - Brom - Iot trang 113 - 114 SGK Giải Hoá học 10 Bài 24: Sơ lược về hợp chất có oxi của clo trang 108 SGK
Giải Hoá học 10 Bài 24: Sơ lược về hợp chất có oxi của clo trang 108 SGK Giải Hoá học 10 Bài 23: Hiđro clorua - Axit clohiđric và muối clorua trang 106 SGK
Giải Hoá học 10 Bài 23: Hiđro clorua - Axit clohiđric và muối clorua trang 106 SGK Giải Hoá học 10 Bài 27: Thực hành số 2 trang 120 SGK
Giải Hoá học 10 Bài 27: Thực hành số 2 trang 120 SGK

