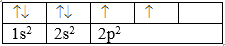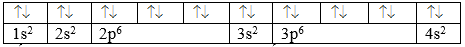Soạn Hóa học 10 nâng cao Bài 10: Sự biến đổi tuần hoàn cấu hình electorn nguyên tử của các nguyên tố hóa học
Với bộ tài liệu giải bài tập SGK Hóa 10 nâng cao Bài 10: Sự biến đổi tuần hoàn cấu hình electorn nguyên tử của các nguyên tố hóa học, hướng dẫn cách giải chi tiết cho từng câu hỏi, từng phần học bám sát nội dung chương trình sách giáo khoa bộ môn Hóa nâng cao lớp 10. Nội dung chi tiết các em xem tại đây.
Giải bài 1 trang 44 SGK Hóa lớp 10 nâng cao
Sự biến thiên tính chất của các nguyên tố thuộc chu kì sau lại được lặp lại giống như chu kì trước là do:
A. sự lặp lại tính kim loại của các nguyên tố ở chu kì sau so với chu kì trước.
B. sự lặp lại tính phi kim của các nguyên tố ở chu kì sau so với chu kì trước.
C. sự lặp lại cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố ở chu kì sau so với chu kì trước.
D. sự lặp lại tính chất hóa học của các nguyên tố ở chu kì sau so với chu kì trước.
Hãy chọn đáp án đúng.
Lời giải:
Chọn C
Giải bài 2 trang 44 SGK Hóa lớp 10 nâng cao
Dựa vào bảng 2.1, hãy cho biết số electron lớp ngoài cùng của nguyên tử các nguyên tố sau đây: H, He, Li, Na, K, Ga, O, S, Cl, Br.
Lời giải:
| Nguyên tố | H | He | Li | Na | K | Ca | O | S | Cl | Br |
| Số electron lớp ngoài cùng | 1 | 2 | 1 | 1 | 1 | 2 | 6 | 6 | 7 | 7 |
Giải bài 3 trang 44 SGK Hóa lớp 10 nâng cao
Cho nguyên tử các nguyên tố có: Z = 8, Z = 9, Z = 17, Z = 19. Hãy xác định số electron lớp ngoài cùng của nguyên tử các nguyên tố đó, số thứ tự nhóm và chu kì chứa các nguyên tố đó.
Lời giải:
| Điện tích hạt nhân | Cấu hình electron | Số e lớp ngoài cùng | Số thứ tự nhóm | Chu kì |
| Z = 8 | 1s22s22p4 | 6 | VIA | 2 |
| Z = 9 | 1s22s22p5 | 7 | VIIA | 2 |
| Z = 17 | 1s22s22p63s23p5 | 7 | VIIA | 3 |
| Z = 19 | 1s22s22p63s23p64s1 | 1 | IA | 4 |
Giải bài 4 trang 44 SGK Hóa lớp 10 nâng cao
Viết cấu hình electron nguyên tử của các nguyên tố có Z = 18 và Z = 19. Tại sao nguyên tố có Z = 18 ở chu kì 3, còn nguyên tố có Z = 19 lại ở chu kì 4?
Lời giải:
Cấu hình electron của nguyên tố có (Z = 18): ls2 2s2 2p6 3s2 3p6
=> Nguyên tố này thuộc chu kì 3 vì có 3 lớp electron.
Cấu hình electron của nguyên tố có (Z = 19): ls2 2s2 2p6 3s2 3p6 4s1
=> Nguyên tố này thuộc chu kì 4 vì có 4 lớp electron.
Giải bài 5 trang 44 SGK Hóa lớp 10 nâng cao
Viết cấu hình electron nguyên tử của các nguyên tố có Z = 20; 21; 24; 29; 30. Cấu hình electron của chúng có đặc điểm gì? Tại sao Cu ở nhóm IB, Zn ở nhóm IIB?
Lời giải:
Cấu hình electron nguyên tử của các nguyên tố:
Z = 20: ls2 2s2 2p6 3s2 3p6 4s2 ;
Z = 21: ls2 2s2 2p6 3s2 3p6 3d1 4s2 ;
Z = 24: ls2 2s2 2p6 3s2 3p6 3d5 4s1 ;
Z = 29: ls2 2s2 2p6 3s2 3p6 3d10 4s1 ;
Z = 30: ls2 2s2 2p6 3s2 3p6 3d10 4s2 ;
Nguyên tử của nguyên tố Z = 20 có electron cuối cùng điền vào phân lớp s của lớp ngoài cùng. Đó là nguyên tố s.
Các nguyên tử của nguyên tố còn lại có electron cuối cùng điền vào phân lớp d sát lớp ngoài cùng. Đó là những nguyên tố d.
Ở nguyên tử của nguyên tố Z = 24 và Z = 29 có sự chuyển 1 electron từ phân lớp 4s của lớp ngoài cùng để đạt cấu hình bán bão hòa (phân lớp 3d có 5e) và bão hòa (phân lớp 3d có đủ 10e).
Những nguyên tố d có phân lớp d đã bão hòa thì số thứ tự nhóm của chúng bằng số electron lớp ngoài cùng. Vì vậy, nguyên tử của nguyên tố Cu (Z = 29) có phân lớp 3d đủ 10 electron và lớp ngoài cùng có 1 electron nên ở nhóm IB và nguyên tử của nguyên tố Zn (Z = 30) có phân lớp 3d đủ 10 electron và lớp ngoài cùng có 2 electron nên ở nhóm IIB.
Giải bài 6 trang 44 SGK Hóa lớp 10 nâng cao
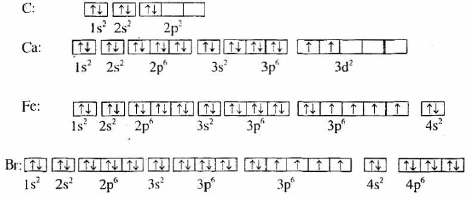
Sự phân bố electron vào các AO của nguyên tử các nguyên tố C, Ca, Fe và Br sau đây đúng hay sai? Nếu sai hãy sửa lại cho đúng.
Lời giải:
Cấu hình electron nguyên tử của nguyên tố C viết sai. Theo quy tắc Hun, 2 electron ở mức 2p phải phân bố trên 2 obitan 2p. Electron được phân bố như sau:
Mức năng lượng 3d cao hơn 4s nên ở nguyên tố Ca, việc viết cấu hình electron đã vi phạm nguyên lí vững bền. Electron được phân bố như sau:
Cấu hình electron nguyên tử của Fe viết đúng.
Cấu hình electron nguyên tử của Br viết thừa 1 electron ở phân lớp 4p. Sửa lại như sau:
►►CLICK NGAY vào nút TẢI VỀ dưới đây để tải về giải bài tập SGK Hóa học lớp 10 nâng cao Bài 10: Sự biến đổi tuần hoàn cấu hình electorn nguyên tử của các nguyên tố hóa học, file PDF hoàn toàn miễn phí.
 Soạn Hóa học 10 nâng cao Bài 14: Luyện tập chương 2
Soạn Hóa học 10 nâng cao Bài 14: Luyện tập chương 2 Soạn Hóa học 10 nâng cao Bài 9: Bảng tuần hoàn các nguyên tố hóa học
Soạn Hóa học 10 nâng cao Bài 9: Bảng tuần hoàn các nguyên tố hóa học Soạn Hóa học 10 nâng cao Bài 15: Bài thực hành số 1
Soạn Hóa học 10 nâng cao Bài 15: Bài thực hành số 1 Soạn Hóa học 10 nâng cao Bài 13: Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học
Soạn Hóa học 10 nâng cao Bài 13: Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học Soạn Hóa học 10 nâng cao Bài 12 (Chính xác nhất)
Soạn Hóa học 10 nâng cao Bài 12 (Chính xác nhất) Soạn Hóa học 10 nâng cao Bài 11: Sự biến đổi một số đại lượng vật lí của các nguyên tố hóa học
Soạn Hóa học 10 nâng cao Bài 11: Sự biến đổi một số đại lượng vật lí của các nguyên tố hóa học Soạn Hóa học 10 nâng cao Bài 10: Sự biến đổi tuần hoàn cấu hình electorn nguyên tử của các nguyên tố hóa học
Soạn Hóa học 10 nâng cao Bài 10: Sự biến đổi tuần hoàn cấu hình electorn nguyên tử của các nguyên tố hóa học