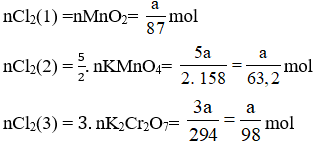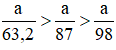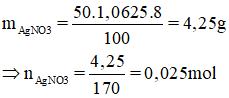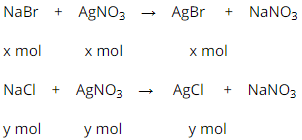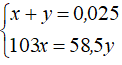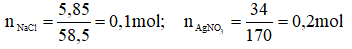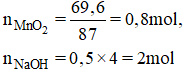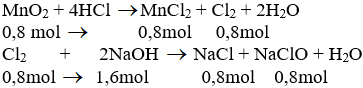Giải Hoá học 10 Bài 26: Luyện tập nhóm halogen trang 118 - 119 SGK
Mời các em học sinh tham khảo ngay nội dung hướng dẫn giải SGK Hóa lớp 10 Bài 26: Luyện tập nhóm halogen được bày chi tiết, dễ hiểu nhất dưới đây sẽ giúp bạn đọc hiểu rõ hơn về bài học này, từ đó chuẩn bị tốt cho tiết học sắp tới nhé.
Giải Bài 1 trang 118 SGK Hoá 10
Dãy aixt nào sau đây được sắp xếp đúng theo thứu tự tính axit giảm dần:
A. HCl, HBr, HI, HF.
B. HBr, HI, HF, HCl.
C. HI, HBr, HCl, HF.
D. HF, HCl, HBr, HI.
Lời giải:
C đúng.
Giải Bài 2 Hoá 10 SGK trang 118
Đổ dung dịch AgNO3 vào dung dịch muối nào sau đây sẽ không có phản ứng:
A. NaF.
B. NaCl.
C. NaBr.
D. NaI.
Lời giải:
A. NaF không phản ứng.
Giải Bài 3 SGK Hoá 10 trang 118
Brom đóng vai trò gì trong phản ứng sau:
SO2 + Br2+ 2H2O → H2SO4 + 2HBr.
A. Chất khử.
B. Chất oxi hóa.
C. Vừa là chất oxi hóa, vừa là chất khử.
D. Không là chất oxi hóa, không là chất khử.
Chọn đáp án đúng.
Lời giải:
B : chất oxi hóa.
Giải Bài 4 trang 28 SGK Hoá 118
Chọn câu đúng khi nói về flo, clo, brom, iot:
A. Flo có tính oxi hóa rất mạnh, oxi hóa mãnh liệt nước.
B. Clo có tính oxi hóa mạnh, oxi hóa được nước.
C. Brom có tính oxi hóa mạnh, nhưng yếu hơn flo và clo, nó cũng oxi hóa được nước.
D. Iot có tính oxi hóa yếu hơn flo, clo, brom nhưng cũng oxi hóa được nước.
Lời giải:
A đúng.
Giải Bài 5 Hoá 10 SGK trang 119
Một nguyên tố halogen có cấu hình electron lớp ngoài cùng của nguyên tử là 4s24p5.
a) Viết cấu hình electron nguyên tử đầy đủ của nguyên tử.
b) Tên, kí hiệu và cấu tạo phân tử của nguyên tố hóa học này.
c) Nêu tính chất hóa học cơ bản của nguyên tố này và dẫn ra những phản ứng hóa học để minh họa.
d) So sánh tính chất hóa học của nguyên tố này với 2 nguyên tử halogen khác đứng trên và dưới nó trong nhóm halogen và dẫn ra phản ứng hóa học để minh họa.
Lời giải:
a) Halogen có cấu hình electron lớp ngoài cùng của nguyên tử là 4s24p5, cấu hình electron đầy đủ là : 1s22s22p63s23p63d104s24p5.
b) Tên nguyên tố là brom, kí hiệu là Br, công thức phân tử là Br2.
c) Tính chất hóa học cơ bản của nguyên tố này là tính oxi hóa.
- Brom phản ứng với nhiều kim loại.
3Br2 + 2Al → 2AlBr3
- Brom tác dụng với nước tương tự clo nhưng khó khăn hơn.
Br2 + H2O ⇆ HBr + HBrO.
- Brom thể hiện tính khử khi tác dụng với chất oxi hóa mạnh
Br2 + 5Cl2 + 6H2O → 2HBrO3 + 10HCl
- Brom có thể occi hóa muối iotua thành iot
Br2 + 2NaI → 2NaBr + I2
d) So sánh tính chất hóa học của brom với clo và iot.
Brom có tính oxi hóa yếu hơn clo nhưng mạnh hơn iot nên:
Cl2 + 2NaBr → 2NaCl + Br2
Br2 + 2NaI → 2NaBr + I2.
Giải Bài 6 trang 119 SGK Hoá 10
Có những chất sau: KMnO4, MnO2, K2Cr2O7 và dung dịch HCl.
a) Nếu các chất oxi hóa có khối lượng bằng nhau thì chọn chất nào có thể điều chế được lượng khí clo nhiều hơn
b) Nếu chất oxi hóa có số mol bằng nhau thì chọn chất nào có thể điều chế được lượng khí clo nhiều hơn?
Hãy trả lời bằng cách tính toán trên cơ sở của các phương trình phản ứng.
Lời giải:
a) Giả sử lấy lượng mỗi chất là a gam
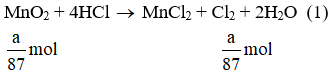
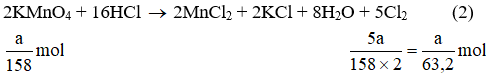
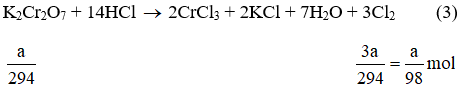
Ta có:
Lượng Cl2 điều chế được từ pt (2) nhiều nhất.
Vậy dùng KMnO4 điều chế được nhiều Cl2 hơn.
b) Nếu lấy số mol các chất bằng a mol
Theo (1) nCl2(1) = nMnO2 = a mol
Theo (2) nCl2(2) = 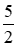
Theo (3) nCl2(3) = 3. nK2Cr2O7 = 3a mol
Ta có: 3a > 2,5a > a.
⇒ lượng Cl2 điều chế được từ pt (3) nhiều nhất.
Vậy dùng K2Cr2O7 được nhiều Cl2 hơn.
Giải Bài 7 Hoá 10 SGK trang 119
Tính khối lượng HCl bị oxi hóa bởi MnO2, biết rằng khí Cl2 sinh ra trong phản ứng đó có thể đẩy được 12,7g I2 từ dung dịch NaI.
Lời giải:
Cl2 + 2NaI → 2NaCl + I2
nI2 = 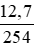
Theo pt: nCl2 = nI2 = 0,05 mol.
4HCl + MnO2 → MnCl2 + Cl2 + 2H2O
nHCl = 4. nCl2 = 4. 0,05 = 0,2 mol.
Khối lượng HCl cần dùng là: mHCl = 0,2 x 36,5 = 7,3g.
Giải Bài 8 SGK Hoá 10 trang 119
Nêu các phản ứng chứng minh rằng tính oxi hóa của clo mạnh hơn brom và iot
Lời giải:
Clo oxi hóa dễ dàng ion Br— trong dung dịch muối bromua và I- trong dung dịch muối iotua:
Cl2 + 2NaBr → 2NaCl + Br2
Cl2 + 2NaI → 2NaCl + I2
Giải Bài 9 trang 119 SGK Hoá 10
Để điều chế flo, người ta phải điện phân dung dịch KF trong hidro florua lỏng đã loại bỏ hết nước. Vì sao phải tránh sự có mặt của nước?
Lời giải:
Khi điện phân hỗn hợp KF trong HF lỏng khan (đã được loại bỏ hết nước). Sở dĩ phải tránh sự có mặt của nước vì flo tác dụng với nước cho thoát ra O2.
2F2 + 2H2O → 4HF + O2
Phản ứng thật ra rất phức tạp : đầu tiên có phản ứng hóa học:
F2 + H2O → 2HF + O
Một số nguyên tử oxi kết hợp với flo cho OF2. Như vậy ta điều chế không được flo nguyên chất.
Giải Bài 10 Hoá 10 SGK trang 119
Trong một dung dịch có hòa tan 2 muối là NaBr và NaCl. Nồng độ phần trăm của mỗi muối trong dụng dịch đều bằng nhau và bằng C%. Hãy xác định nồng độ C% của 2 muối trong dung dịch biết rằng 50g dung dịch hai muối nói trên tác dụng vừa đủ với 50ml dung dịch AgNO3 8%, có khối lượng riêng D = 1,0625 g/cm3.
Lời giải:
Phương trình hóa học của phản ứng:
Biết nồng độ phần trăm của mỗi muối trong dung dịch bằng nhau và khối lượng dung dịch là 50g, do đó khối lượng NaCl bằng khối lượng NaBr.
Gọi nNaBr = x, nNaCl = y.
Theo pt: nNaBr = nAgNO3; nNaCl = nAgNO3
⇒ nNaBr + nNaCl = nAgNO3
Ta có hệ phương trình đại số:
Giải ra, ta có x ≈ 0,009 mol
→ mNaBr = mNaCl = 103 x 0,009 = 0,927g
Giải Bài 11 trang 119 SGK Hoá 10
Cho 300ml một dung dịch có hòa tan 5,85g NaCl tác dụng với 200ml dung dịch có hòa tan 34g AgNO3, người ta thu được một kết tủa và nước lọc.
a) Tính khối lượng chất kết tủa thu được.
b) Tính nồng độ mol chất còn lại trong nước lọc. Cho rằng thể tích nước lọc thu được không thay đổi đáng kể
Lời giải:
a) Phương trình hóa học của phản ứng:
NaCl + AgNO3 → AgCl↓ + NaNO3
Theo pt: nAgNO3 pư = nAgCl = nNaCl = 0,1 mol
b) Vdd = 300 + 200 = 500 ml
nAgNO3 dư = 0,2 – 0, 1 = 0,1 mol; nNaNO3 = nNaCl = 0,1 mol
CM(NaNO3) = CM(AgNO3) = 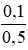
Giải Bài 12 Hoá 10 SGK trang 119
Cho 69,6g MnO2 tác dụng với dung dịch HCl đặc, dư. Dẫn khí thoát ra đi vào 500ml dung dịch NaOH 4M (ở nhiệt độ thường).
a) Viết phương trình hóa học của phản ứng xảy ra.
b) Xác định nồng độ mol/l của những chất có trong dung dịch sau phản ứng. Biết rằng tinh thể của dung dịch sau phản ứng thay đổi không đáng kể
Lời giải:
a) Phương trình hóa học của phản ứng:
b) Theo pt (1): nCl2 = nMnCl2 = nMnO2 = 0,8 mol
Theo pt (2): nNaCl = nNaClO = nCl2 = 0,8 mol
nNaOH pư = 2. nCl2 = 2. 0,8 = 1,6 mol
⇒ nNaOH dư = 2 - 1,6 = 0,4 mol
Nồng độ mol/l của các chất trong dung dịch sau phản ứng:
CM (NaCl) = CM (NaClO) = CM(MnCl2) = 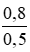
CM (NaOH)dư = 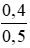
Giải Bài 13 SGK Hoá 10 trang 119
Khí oxi có lẫn tạp chất là khí clo. Làm thế nào để loại bỏ tạp chất đó.
Lời giải:
Cho hỗn hợp khí qua dung dịch NaOH, khi clo tác dụng với dung dịch NaOH, ta thu được khí O2.
Cl2 + 2NaOH → NaCl + NaClO + H2O.
►► CLICK NGAY vào đường dẫn dưới đây để TẢI VỀ lời giải bài tập SGK Hóa 10 Bài 26: Luyện tập nhóm halogen, chi tiết, đầy đủ nhất file word, file pdf hoàn toàn miễn phí từ chúng tôi, hỗ trợ các em ôn luyện giải đề đạt hiệu quả nhất.
 Soạn Hóa 10 Bài 21: Khái quát về nhóm Halogen đầy đủ nhất
Soạn Hóa 10 Bài 21: Khái quát về nhóm Halogen đầy đủ nhất Soạn Hóa học 10 Bài 22: Clo chi tiết nhất
Soạn Hóa học 10 Bài 22: Clo chi tiết nhất Giải Hoá học 10 Bài 28: Bài thực hành số 3 trang 120 SGK
Giải Hoá học 10 Bài 28: Bài thực hành số 3 trang 120 SGK Giải Hoá học 10 Bài 26: Luyện tập nhóm halogen trang 118 - 119 SGK
Giải Hoá học 10 Bài 26: Luyện tập nhóm halogen trang 118 - 119 SGK Giải Hoá học 10 Bài 25: Flo - Brom - Iot trang 113 - 114 SGK
Giải Hoá học 10 Bài 25: Flo - Brom - Iot trang 113 - 114 SGK Giải Hoá học 10 Bài 24: Sơ lược về hợp chất có oxi của clo trang 108 SGK
Giải Hoá học 10 Bài 24: Sơ lược về hợp chất có oxi của clo trang 108 SGK Giải Hoá học 10 Bài 23: Hiđro clorua - Axit clohiđric và muối clorua trang 106 SGK
Giải Hoá học 10 Bài 23: Hiđro clorua - Axit clohiđric và muối clorua trang 106 SGK Giải Hoá học 10 Bài 27: Thực hành số 2 trang 120 SGK
Giải Hoá học 10 Bài 27: Thực hành số 2 trang 120 SGK