Soạn Hóa học 10 Bài 22: Clo chi tiết nhất
Để quá trình tiếp thu kiến thức mới trở nên dễ dàng và đạt hiệu quả nhất, trước khi bắt đầu bài học mới các em cần có sự chuẩn bị nhất định qua việc tổng hợp nội dung kiến thức lý thuyết trọng tâm, sử dụng những kiến thức hiện có thử áp dụng giải các bài tập ứng dụng, trả lời câu hỏi liên quan. Dưới đây chúng tôi đã soạn sẵn Hóa học 10 Bài 22: Clo chi tiết nhất, giúp các em tiết kiệm thời gian. Nội dung chi tiết được chia sẻ dưới đây.
Bài 22: Clo
Bài tập SGK
Bài 1 (trang 101 SGK Hóa 10):
Trong phòng thí nghiệm, khí clo thường được điều chế bằng cách oxi hóa hợp chất nào sau đây:
A. NaCl.
B. HCl.
C. KClO3.
D. KMnO4.
Hướng dẫn giải chi tiết:
Đáp án B. HCl đúng.
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
Bài 2 (trang 101 SGK Hóa 10):
Cho biết tính chất hóa học cơ bản của nguyên tố clo. Giải thích vì sao nguyên tố clo có tính chất hóa học cơ bản đó? Cho thí dụ minh họa.
Hướng dẫn giải chi tiết:
Tính chất hóa học cơ bản của clo: Clo là chất oxi hóa mạnh.
- Tác dụng với kim loại : clo oxi hóa trực tiếp hầu hết các kim loại tạo muối clorua, phản ứng xảy ra ở nhiệt độ thường hoặc không cao lắm, tốc độ nhanh, tỏa nhiều nhiệt.
2Fe + 3Cl2 ->(nhiệt độ) 2FeCl3
- Tác dụng với hiđro: Phản ứng xảy ra khi chiếu sáng bởi ánh sáng mặt trời:
H2 + Cl2 → 2HCl.
- Tác dụng với nước:
Trong phản ứng với nước, clo vừa là chất oxi hóa vừa là chất khử.
Cl2 + H2O ⇆ HCl + HClO
Sở dĩ có những tính chất hóa học cơ bản trên vì khi tham gia phản ứng, nguyên tử clo dễ nhận thêm 1 electron để thành ion Cl-. Vì vậy tính chất hóa học cơ bản của clo là tính oxi hóa mạnh.
Bài 3 (trang 101 SGK Hóa 10):
Dẫn khi clo vào nước, xảy ra hiện tượng vật lí hay hóa học? Giải thích.
Hướng dẫn giải chi tiết:
Dẫn khí clo vào nước, xảy ra vừa là hiện tượng vật lí vừa là hiện tượng hóa học. Khi tan vào nước, một phần clo tác dụng với nước.
Cl2 + H2O ⇆ HCl + HClO.
Bài 4 (trang 101 SGK Hóa 10):
Nêu những ứng dụng thực tế của khí clo.
Hướng dẫn giải chi tiết:
Những ứng dụng thực tế của clo:
1. Khí clo được dùng để tiệt trùng nước sinh hoạt, hòa tan vào nước một lượng nhỏ khí clo để diệt vi khuẩn gây bệnh.
2. Khí clo được dùng để sản xuất các chất tẩy trắng, sát trùng như nước Gia – ven, clorua vôi và sản xuất những hóa chất trong công nghiệp như HCl, KClO3.
3. Một lượng lớn clo được dùng để chế những dung môi công nghiệp như cacbon tetra clorua (CCl4) sản xuất nhiều chất polime như nhựa PVC, cao su tổng hợp, tơ clorin v.v ...
Bài 5 (trang 101 SGK Hóa 10):
Cân bằng các phương trình phản ứng oxi hóa – khử sau bằng phương pháp thăng bằng electron:
a) KMnO4 + HCl → KCl + MnCl2 + Cl2 + H2O.
b) HNO3 + HCl → NO + Cl2 + H2O.
c) HClO3 + HCl → Cl2 + H2O.
d) PbO2 + HCl → PbCl2 + Cl2 + H2O.
Hướng dẫn giải chi tiết:
Cân bằng các phản ứng oxi hóa – khử sau bằng phương pháp thăng bằng electron:
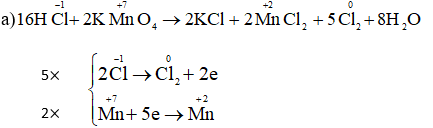
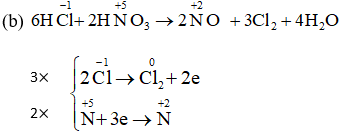
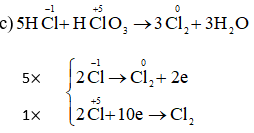
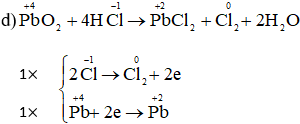
Lý thuyết trọng tâm
I. Tính chất vật lý
- Clo là chất khí, màu vàng, mùi xốc, độc và nặng hơn không khí.
- Cl2 có một liên kết cộng hóa trị, dễ dàng tham gia phản ứng,là một chất oxi hóa mạnh.
- Tham gia các phản ứng Clo là chất oxi hoá, tuy nhiên clo cũng có khả năng đóng vai trò là chất khử.
II. Tính chất hoá học
1. Tác dụng với kim loại
Đa số kim loại và có to để khơi màu phản ứng tạo muối clorua (có hoá trị cao nhất )
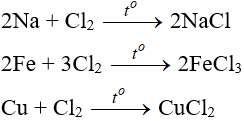
2. Tác dụng với phim kim
(cần có nhiệt độ hoặc có ánh sáng)
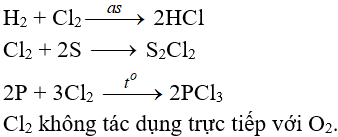
3. Tác dụng với nước và dung dịch kiềm
Cl2 tham gia phản ứng với vai trò vừa là chất ôxi hóa, vừa là chất khử.
a. Tác dụng với nuớc
Khi hoà tan vào nước, một phần Clo tác dụng (Thuận nghịch)
Cl20 + H2O → HCl + HClO (Axit hipoclorơ)
Axit hipoclorơ có tính oxy hoá mạnh, nó phá hửy các màu vì thế nước clo hay clo ẩm có tính tẩy màu do.
b. Tác dụng với dung dịch bazơ
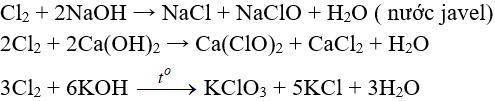
4. Tác dụng với muối của các halogen khác
Cl2 + 2NaBr → 2NaCl + Br2
Cl2 + 2FeCl2 → 2FeCl3
3Cl2 + 6FeSO4 → 2Fe2(SO4)3 + 2FeCl3
Cl2 + 2KI → 2KCl + I2
5. Tác dụng với chất khử khác
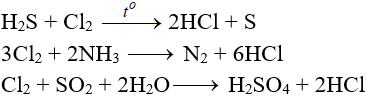
6. Phản ứng thế, phản ứng cộng, phản ứng phân huỷ với một số hợp chất hữu cơ
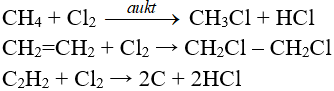
III. Ứng dụng
Clo có vai trò rất quan trọng trong công nghiệp chất:
- Dùng để sát trùng nước khi xử lí nước thải.
- Tẩy trắng sợi, giấy, vải.
- Là nguyên liệu để sản xuất nhiều hợp chất vô cơ và hữu cơ. Sản phẩm hữu cơ chứa clo có ý nghĩa to lớn trong công nghiêp.
IV. Trạng thái tự nhiên
- Trong tự nhiên Clo có 2 đồng vị 3517Cl (75%) và 3717Cl (25%) ⇒ M−Cl = 35,5.
- Do hoạt động hóa học mạnh nên clo chỉ tồn tại trong tự nhiên ở dạng hợp chất, chủ yếu là muối clorua.
- Hợp chất quan trọng nhất của clo là natri clorua.
V. Điều chế
Nguyên tắc là khử các hợp chất Cl- tạo Cl0
a. Trong phòng thí nghiệm
Cho HCl đậm đặc tác dụng với các chất ôxi hóa mạnh
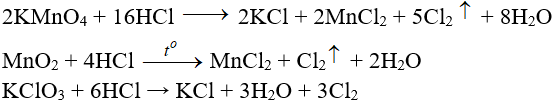
b. Trong công nghiệp
Dùng phương pháp điện phân
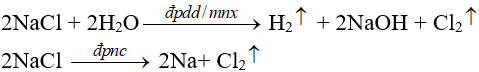
(bổ sung thêm kiến thức về điện phân)
(nếu quá trình điện phân không có màng ngăn thì sản phẩm thu được là dung dịch nước javel)
Ngoài ra còn có thể từ HCl và O2 có xúc tác là CuCl2 ở 400oC.
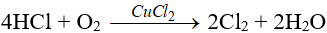
Bộ câu hỏi trắc nghiệm
Câu 1: Cho clo vào nước, thu được nước clo. Biết clo tác dụng không hoàn toàn với nước. Nước clo là hỗn hợp gồm các chất :
A. HCl, HClO
B. HClO, Cl2, H2O
C. H2O, HCl, HClO
D. H2O, HCl, HClO, Cl2
Đáp án: D
Câu 2: Trong phòng thí nghiệm, người ta thường điều chế clo bằng cách
A. điện phân nóng chảy NaCl.
B. cho dung dịch HCl đặc tác dụng với MnO2, đun nóng.
C. điện phân dung dịch NaCl có màng ngăn.
D. cho F2 đẩy Cl2 ra khỏi dung dịch NaCl.
Đáp án: B
Câu 3: Cho kim loại M tác dụng với Cl2 được muối X; cho kim lọai M tác dụng với dung dịch HCl được muối Y. Nếu cho dung dịch muối Y tác dụng với Cl2 cũng thu được muối X. Kim loại M có thể là
A. Mg B. Zn C. Al D. Fe
Đáp án: D
Câu 4: Chất dùng để làm khô khí Cl2 ẩm là
A. dung dịch H2SO4 đậm đặc.
B. Na2SO3 khan.
C. CaO.
D. dung dịch NaOH đặc.
Đáp án: A
Câu 5: Cho 29,2 gam HCl tác dụng hết với KMnO4, thu được V lít khí Cl2 (đktc). Giá trị của V là
A. 8,96 B. 17,92 C. 5,60 D. 11,20
Đáp án: C
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2O
⇒ nHCl = 29,2/36,5 = 0,8 (mol) ⇒ nCl2 = 0,8.5/16 = 0,25
V = 0,25 . 22,4 = 5,6 (l)
Câu 6: Đốt cháy sắt trong khí clo, người ta thu được 32,5 gam muối. Thể tích khí clo (đktc) đã tham gia phản ứng là
A. 6,72 lít. B. 13,44 lít. C. 4,48 lít. D. 2,24 lít.
Đáp án: A
nFeCl3 = 32,5/162,5 = 0,2 (mol)
Bảo toàn nguyên tố Cl
2nCl2 = 3nFeCl3 ⇒ nCl2 = 0,3 (mol) ⇒ V = 0,3 .22,4 = 6,72 (l)
Câu 7: Đốt cháy 11,9 gam hỗn hợp gồm Zn, Al trong khí Cl2 dư. Sau khi các phản ứng xảy ra hoàn toàn, thu được 40,3 gam hỗn hợp muối. Thể tích khí Cl2 (đktc) đã phản ứng là
A. 17,92 lít. B. 6,72 lít. C. 8,96 lít. D. 11,20 lít.
Đáp án: C
Bảo toàn khối lượng:
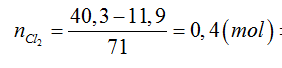
⇒ V = 0,4 . 22,4 = 8,96l
Câu 8: Cho 17,4 gam MnO2 tác dụng hết với dung dịch HCl đặc (dư), đun nóng. Cho toàn bộ khí clo thu được tác dụng hết với một kim loại M có hóa trị 2 thì thu được 22,2 gam muối. Kim loại M là
A. Ca B. Zn C. Cu D. Mg
Đáp án: A
Bảo toàn electron: nMCl2 = nMnO2 = 17,4/87 = 0,2 (mol)
⇒ 0,2 (M + 71) = 22,2 ⇒ M = 40 (Ca)
Câu 9: Nguyên tố Cl ở ô thứ 17 trong bảng tuần hoàn, cấu hình electron của ion Cl- là :
A. 1s22s22p63s23p4.
B. 1s22s22p63s23p2.
C. 1s22s22p63s23p6.
D. 1s22s22p63s23p5.
Đáp án: C
Câu 10: Cho 7,84 lít hỗn hợp khí X (đktc) gồm Cl2 và O2 phản ứng vừa đủ với 11,1 gam hỗn hợp Y gồm Mg và Al, thu được 30,1 gam hỗn hợp Z. Phần trăm khối lượng của Al trong Y là
A. 75,68%. B. 24,32%.
C. 51,35%. D. 48,65%.
Đáp án: B
nCl2 = x mol; nO2 = y mol
⇒ x + y = 0,35 mol (1)
Áp dụng định luật bảo toàn khối lượng: mCl2 + mO2 = mZ – mY = 19g
⇒ 71x + 32y = 19 (2)
Từ (1)(2) ⇒ x = 0,2; y = 0,15
Đặt nMg = a mol; nAl = b mol
⇒ 24a + 27b = 11,1g (3)
Bảo toàn e: 2nMg + 3nAl = 2nCl2 + 4nO2
⇒ 2a + 3b = 1 (4)
Từ (3)(4) ⇒ a = 0,35; b = 0,1
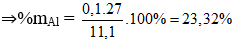
Câu 11: Sục Cl2 vào nước, thu được nước clo màu vàng nhạt. Trong nước clo có chứa các chất là :
A. Cl2, H2O.
B. HCl, HClO.
C. HCl, HClO, H2O.
D. Cl2, HCl, HClO, H2O.
Đáp án: D
Câu 12: Hoà tan khí Cl2 vào dung dịch KOH đặc, nóng, dư. Dung dịch thu được có các chất thuộc dãy nào dưới đây ?
A. KCl, KClO3, Cl2.
B. KCl, KClO3, KOH, H2O.
C. KCl, KClO, KOH, H2O.
D. KCl, KClO3.
Đáp án: B
Câu 13: Trong các halogen, clo là nguyên tố
A. Có độ âm điện lớn nhất.
B. Có tính phi kim mạnh nhất.
C. Tồn tại trong vỏ Trái Đất (dưới dạng các hợp chất) với trữ lượng lớn nhất.
D. Có số oxi hóa –1 trong mọi hợp chất.
Đáp án: C
Câu 14: Thể tích dung dịch NaOH 1M để tác dụng hoàn toàn với 1,12 lít khí clo là: (đktc, Giả thiết thể tích dung dịch thay đổi không đáng kể)
A. 100ml B. 50ml
C. 500ml D. 200ml
Đáp án: A
2NaOH + Cl2 → NaClO + NaCl + H2O
nNaOH = 2 nCl2 = 2. 0,05 = 0,1 mol
⇒ VNaOH = 0,1 : 1 = 0,1 lít = 100ml
Câu 15: Cho 10,8 gam kim loại M hóa trị III tác dụng với khí clo dư thì thu được 53,4 gam muối. Kim loại M là:
A. Al B. Cr
C. Fe D.Ni
Đáp án: A
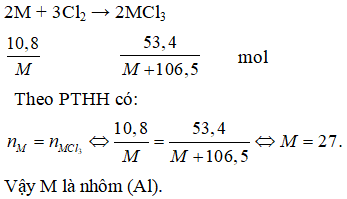
File tải hướng dẫn soạn Hóa 10 Bài 22: Clo
Hy vọng tài liệu sẽ hữu ích cho các em học sinh và quý thầy cô giáo tham khảo.
►Ngoài ra các em học sinh và thầy cô có thể tham khảo thêm nhiều tài liệu hữu ích hỗ trợ ôn luyện thi môn Hóa như đề kiểm tra học kì, 1 tiết, 15 phút trên lớp, hướng dẫn giải sách giáo khoa, sách bài tập được cập nhật liên tục tại chuyên trang của chúng tôi.
 Soạn Hóa 10 Bài 21: Khái quát về nhóm Halogen đầy đủ nhất
Soạn Hóa 10 Bài 21: Khái quát về nhóm Halogen đầy đủ nhất Soạn Hóa học 10 Bài 22: Clo chi tiết nhất
Soạn Hóa học 10 Bài 22: Clo chi tiết nhất Giải Hoá học 10 Bài 28: Bài thực hành số 3 trang 120 SGK
Giải Hoá học 10 Bài 28: Bài thực hành số 3 trang 120 SGK Giải Hoá học 10 Bài 26: Luyện tập nhóm halogen trang 118 - 119 SGK
Giải Hoá học 10 Bài 26: Luyện tập nhóm halogen trang 118 - 119 SGK Giải Hoá học 10 Bài 25: Flo - Brom - Iot trang 113 - 114 SGK
Giải Hoá học 10 Bài 25: Flo - Brom - Iot trang 113 - 114 SGK Giải Hoá học 10 Bài 24: Sơ lược về hợp chất có oxi của clo trang 108 SGK
Giải Hoá học 10 Bài 24: Sơ lược về hợp chất có oxi của clo trang 108 SGK Giải Hoá học 10 Bài 23: Hiđro clorua - Axit clohiđric và muối clorua trang 106 SGK
Giải Hoá học 10 Bài 23: Hiđro clorua - Axit clohiđric và muối clorua trang 106 SGK Giải Hoá học 10 Bài 27: Thực hành số 2 trang 120 SGK
Giải Hoá học 10 Bài 27: Thực hành số 2 trang 120 SGK

