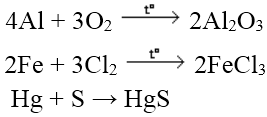Giải Hóa 12 Bài 18: Tính chất của kim loại. Dãy điện hóa của kim loại
Để quá trình tiếp thu kiến thức mới trở nên dễ dàng và đạt hiệu quả nhất, trước khi bắt đầu bài học mới các em cần có sự chuẩn bị nhất định qua việc tổng hợp nội dung kiến thức lý thuyết trọng tâm, sử dụng những kiến thức hiện có thử áp dụng giải các bài tập ứng dụng, trả lời câu hỏi liên quan. Dưới đây chúng tôi đã soạn sẵn Lời giải Bài 18: Tính chất của kim loại. Dãy điện hóa của kim loại đầy đủ nhất, giúp các em tiết kiệm thời gian. Nội dung chi tiết được chia sẻ dưới đây.
Bài 18: Tính chất của kim loại. Dãy điện hóa của kim loại
Bài tập ứng dụng:
Bài 1 (trang 88 SGK Hóa 12):
Giải thích vì sao kim loại đề có tính chất vật lý chung là dẫn điện, dẫn nhiệt, dẻo và ánh kim?
Hướng dẫn giải chi tiết:
Tính chất vật lý chung của kim loại có được là do trong cấu tạo mạng tinh thể kim loại có các electron tự do chuyển động trong mạng tinh thể kim loại.
Bài 2 (trang 88 SGK Hóa 12):
Tính chất hóa học cơ bản của kim loại là gì và vì sao kim loại lại có tính chất đó?
Hướng dẫn giải chi tiết:
Tính chất hóa học chung của kim loại là tính khử
M – ne → Mn+
Bởi vì:
Nguyên tử kim loại có số electron hóa trị ít 1,2,3 electron.
Trong cùng một chu kỳ bán kính nguyên tử kim loại lớn, điện tích hạt nhân nhỏ.
Năng lượng ion hóa nguyên tử kim loại nhỏ.
Vì vậy lực liên kết giữa hạt nhân với các electron hóa trị của kim loại là yếu nên chúng dễ tách ra khỏi nguyên tử. Kim loại thể hiện tính khử.
Bài 3 (trang 88 SGK Hóa 12):
Thủy ngân dễ bay hơi và rất độc. Nếu chẳng may nhiệt kế thủy ngân bị vỡ thì có thể dùng chất nào trong các chất sau để khử độc thủy ngân?
A. Bột sắt.
B. Bột lưu huỳnh.
C. Natri.
D. Nước.
Hướng dẫn giải chi tiết:
Đáp án B.
Vì Hg độc nhưng khi Hg + S → HgS (không độc)
Bài 4 (trang 89 SGK Hóa 12):
Dung dịch FeSO4 có lẫn tạp chất là CuSO4. Hãy giới thiệu phương pháp hóa học đơn giản để có thể loại được tạp chất. Giải thích việc làm viết phương trình phản ứng dạng phân tử và ion thu gọn.
Hướng dẫn giải chi tiết:
Cho một thanh sắt sạch vào dung dịch có phản ứng
Fe + CuSO4 → FeSO4 + Cu
Toàn bộ Cu thoát ra bám trên bề mặt thanh sắt, lấy thanh sắt ra ta còn lại dung dịch chỉ có FeSO4
Fe + CuSO4 → FeSO4 + Cu
Fe + Cu2+→ Fe2++ Cu
Bài 5 (trang 9 SGK Hóa 12):
Nhúng một lá sắt nhỏ vào dung dịch chứa một trong những chất sau: FeCl3, AlCl3, CuSO4, Pb(NO3)2, NaCl, HCl, HNO3, H2SO4(đặc nóng), NH4NO3. Số trường hợp phản ứng tạo muối Fe(II) là
A. 3.
B. 4.
C. 5.
D. 6.
Hướng dẫn giải chi tiết:
Chọn B.
Các chất là FeCl3, CuSO4, Pb(NO3)2, HCl
Bài 6 (trang 89 SGK Hóa 12):
Cho 5,5 gam hỗn hợp Al và Fe (trong đó số mol Al gấp đôi số mol Fe) vào 300 ml dung dịch AgNO3 1M. Khuấy kỹ đến phản ứng hoàn toàn thu m gam chất rắn. Giá trị của m là :
A. 33,95 g
B. 35,2g
C. 39,35g
D. 35,39g
Hướng dẫn giải chi tiết:
Đáp án B.
Các phương trình hóa học có thể xảy ra :
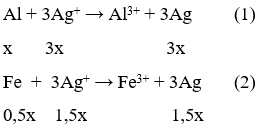
nAgNO3 = 0,3. 1 = 0,3 mol
Gọi số mol Al là x thì số mol Fe là 0,5x
Theo đề bài ta có: 27x + 56. 0,5x = 5,5 (1) suy ra x = 0,1 mol
Theo pt(1) nAgNO3 = 3. nAl = 3. 0,1 = 0,3 mol do đó chỉ xảy ra phản ứng (1).
Chất rắn thu được sau phản ứng là Ag và Fe
Khối lượng chất rắn = mAg + mFe = 0,3. 108 + 0,1. 0,5. 56 = 35,2 (g)
Fe + 2FeCl3 → 3FeCl2
Fe + CuSO4 → FeSO4 + Cu
Fe + Pb(NO3)2 → Fe(NO3)2 + Pb
Fe + 2HCl → FeCl2 + H2
Bài 7 (trang 89 SGK Hóa 12):
Hãy sắp xếp theo chiều giảm tính khử và chiều tăng tính oxi hoá của các nguyên tử và ion trong hai trường hợp sau đây:
a) Fe, Fe2+, Fe3+, Zn, Zn2+, Ni, Ni2+, H, H+, Hg, Hg2+, Ag, Ag+.
b) Cl, Cl–, Br, Br–, F, F–, I, I–.
Hướng dẫn giải chi tiết:
a) Giảm tính khử: Zn > Fe > Ni > H > Hg > Ag
Tăng tính oxi hóa: Zn2+ < Fe2+ < Ni2+ < H+ < Hg2+ < Fe3+ < Ag+
b) Giảm tính khử: I– > Br– > Cl– > F–
Tăng tính oxi hóa: I < Br < Cl < F
Bài 8 (trang 89 SGK Hóa 12):
Những tính chất vật lý chung của kim loại (dẫn điện, dẫn nhiệt, dẻo, ánh kim ) gây ra chủ yếu bởi:
A. Cấu tạo mạng tinh thể của kim loại.
B. Khối lượng riêng của kim loại.
C. Tính chất của kim loại.
D. Các electron tự do trong tinh thể kim loại.
Hướng dẫn giải chi tiết:
Đáp án D.
Lý thuyết trọng tâm:
Tính chất của kim loại:
1. Vị trí, cấu tạo của kim loại
a. Vị trí
- Nhóm IA (trừ H), nhóm IIA: các kim loại này là những nguyên tố s
- Nhóm IIIA (trừ B), một phần của các nhóm IVA, VA, VIA: các kim loại này là những nguyên tố p
- Các nhóm B (từ IB đến VIIIB): các kim loại chuyển tiếp, chúng là những nguyên tố d
- Họ lantan và actini (xếp riêng thành hai hàng ở cuối bảng): các kim loại thuộc hai họ này là những nguyên tố f
b. Cấu tạo
- Cấu tạo nguyên tử kim loại
+ Hầu hết các nguyên tử kim loại có 1, 2 hoặc 3 electron ở lớp ngoài cùng
+ Bán kính nguyên tử của các nguyên tố kim loại nhìn chung lớn hơn bán kính nguyên tử các nguyên tố phi kim
- Cấu tạo mạng tinh thể kim loại
Có ba kiểu mạng tinh thể kim loại đặc trưng là lập phương tâm khối, lập phương tâm diện và lục phương
- Liên kết kim loại
Là liên kết hóa học hình thành bởi lực hút tĩnh điện giữa ion dương kim loại nằm ở các nút mạng tinh thể và các electron tự do di chuyển trong toàn bộ mạng lưới tinh thể kim loại.
2. Tính chất vật lý
- Kim loại có tính chất vật lí chung là dẻo, dẫn điện, dẫn nhiệt và có ánh kim.
- Một số tính chất vật lí riêng:
* Tỉ khối: của các kim loại rất khác nhau nhưng thường dao động từ 0,5 (Li) đến 22,6 (Os). Thường thì:
+ d < 5: kim loại nhẹ (K, Na, Mg, Al).
+ d > 5: kim loại nặng (Zn, Fe...).
* Nhiệt độ nóng chảy: biến đổi từ -39oC (Hg) đến 3410oC (W). Thường thì:
+ t < 10000C: kim loại dễ nóng chảy.
+ t > 15000C: kim loại khó nóng chảy (kim loại chịu nhiệt).
* Tính cứng: Biến đổi từ mềm đến rất cứng.
Tỷ khối, nhiệt độ nóng chảy và tính cứng của kim loại phụ thuộc vào nhiều yếu tố như kiểu mạng tinh thể; mật độ e; khối lượng mol của kim loại...
3. Tính chất hóa học
Tính chất đặc trưng của kim loại là tính khử (nguyên tử kim loại dễ bị oxi hóa thành ion dương): M → Mn+ + ne
a. Tác dụng với phi kim
Hầu hết các kim loại khử được phi kim điển hình thành ion âm
Ví dụ:
b. Tác dụng với axit
- Đối với dung dịch HCl, H2SO4 loãng:
M + nH+ → Mn+ + n/2H2
(M đứng trước hiđro trong dãy thế điện cực chuẩn)
- Đối với H2SO4 đặc, HNO3 (axit có tính oxi hóa mạnh):
+ Kim loại thể hiện nhiều số oxi hóa khác nhau khi phản ứng với H2SO4 đặc, HNO3 sẽ đạt số oxi hóa cao nhất.
+ Hầu hết các kim loại phản ứng được với HNO3 và H2SO4 đặc (trừ Pt, Au)
Lưu ý: Fe, Al, Cr bị thụ động hóa trong H2SO4 và HNO3 đặc nguội.
Khi đó S
+6 H2SO4 bị khử thành S+4 (SO2); So hoặc S-2 (H2S)
Trong HNO3 đặc N+5 bị khử thành N+4 (NO2)
Với HNO3 loãng N+5 bị khử thành N+2(NO); N+1 (N2O); No (N2); N-3 (NH4+)
+ Các kim loại có tính khử càng mạnh thường cho sản phẩm khử có số oxi hóa càng thấp. Các kim loại như Na, K... sẽ gây nổ khi tiếp xúc với các dung dịch axit
Ví dụ:
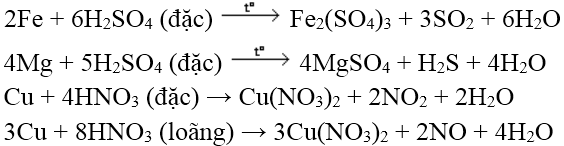
c. Tác dụng với dung dịch muối
- Với Na, K, Ca và Ba phản ứng với nước trước sau đó dung dịch kiềm tạo thành sẽ phản ứng với muối.
- Với các kim loại không tan trong nước, kim loại hoạt động đẩy được kim loại kém hoạt động ra khỏi dung dịch muối của chúng theo quy tắc α.
Fe + CuSO4 → FeSO4 + Cu
Chú ý:
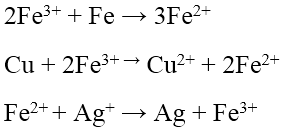
d. Tác dụng với dung dịch kiềm
Các kim loại mà hiđroxit của chúng có tính lưỡng tính như Al, Zn, Be, Sn, Pb... tác dụng được với dung dịch kiềm (đặc).
2Al + 6H2O + 2NaOH → 2Na[Al(OH)4] + 3H2
e. Tác dụng với oxit kim loại
Các kim loại mạnh khử được các oxit kim loại yếu hơn ở nhiệt độ cao thành kim loại
Ví dụ:
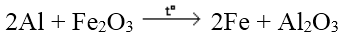
4. Điều chế
Nguyên tắc điều chế: Khử ion kim loại thành kim loại
Mn+ + ne → M
* Một số phương pháp điều chế
a. Phương pháp nhiệt luyện
- Nguyên tắc: dùng chất khử CO, C, Al, H2 khử oxit kim loại ở nhiệt độ cao.
- Phạm vi sử dụng: thường dùng trong công nghiệp với kim loại sau Al.
Ví dụ:
PbO + C → Pb + CO
Fe2O3 + 3CO → 2Fe + 3CO2
b. Phương pháp thủy luyện
- Nguyên tắc: Dùng dung dịch thích hợp (HCl, HNO3, nước cường toan, CN-...) hòa tan nguyên liệu sau đó lấy kim loại mạnh (không tan trong nước) đẩy kim loại yếu khỏi dung dịch của nó.
- Phạm vi sử dụng: thường dùng trong phòng thí nghiệm để điều chế các kim loại sau Mg (thường là kim loại yếu).
Ví dụ:
Vàng lẫn trong đất đá có thể hòa tan dần trong dung dịch NaCN cùng với oxi của không khí, được dung dịch muối phức của vàng:
4Au + 8NaCN + O2 + 2H2O → 4Na[Au(CN)2] + 4NaOH
Sau đó, ion Au3+ trong phức được khử bằng kim loại Zn:
Zn + 2Na[Au(CN)2] → Na2[Zn(CN)4] + 2Au
c. Phương pháp điện phân
- Điện phân nóng chảy
+ Nguyên tắc: Dùng dòng điện một chiều khử ion kim loại trong chất điện li nóng chảy (muối halogenua, oxit, hidroxit).
+ Phạm vi sử dụng: có thể dùng để điều chế tất cả các kim loại nhưng thường dùng với kim loại mạnh: K, Na, Mg, Ca, Ba và Al.
- Điện phân dung dịch
+ Nguyên tắc: Dùng dòng điện một chiều khử ion kim loại yếu trong dung dịch muối của nó.
+ Phạm vi sử dụng: Dùng điều chế các kim loại yếu.
Dãy điện hóa của kim loại
I. Khái niệm về cặp oxi hóa – khử của kim loại
1. Cặp oxi hoá – khử của kim loại
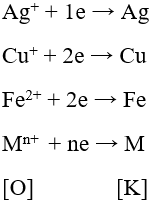
- Dạng oxi hoá và dạng khử của cùng một nguyên tố kim loại tạo nên cặp oxi hoá – khử của kim loại.
Ví dụ: Cặp oxi hoá – khử Ag+/Ag; Cu2+/Cu; Fe2+/Fe
2. So sánh tính chất của các cặp oxi hoá – khử
Ví dụ: So sánh tính chất của hai cặp oxi hoá – khử Cu2+/Cu và Ag+/Ag.
Cu + 2Ag+ → Cu2+ + 2Ag
Kết luận: Tính khử: Cu > Ag
Tính oxi hoá: Ag+ > Cu2+
II. Pin điện hóa
a. Cấu tạo
Là 1 thiết bị gồm: 2 lá kim loại, mỗi lá được nhúng vào 1 dd muối có chứa cation của kim loại đó; 2 dd này được nối với nhau bằng 1 cầu muối (dd điện li trơ: NH4NO3, KNO3)
- Suất điện động của pin điện hoá (VD: Zn - Cu)
Epin = 1,10V
b. Giải thích
- Điện cực Zn (cực âm) là nguồn cung cấp e, Zn bị oxi hoá thành Zn2+ tan vào dung dịch:
Zn → Zn2+ + 2e
- Điện cực Cu (cực dương) các e đến cực Cu, ở đây các ion Cu2+ bị khử thành kim loại Cu bám trên bề mặt lá đồng.
Cu2+ + 2e → Cu
- Vai trò của cầu muối: Trung hòa điện tích của 2 dung dịch
+ Cation NH4+ (hoặc K+) và Zn2+ di chuyển sang cốc đựng dung dịch CuSO4
+ Ngược lại: các anion NO3- và SO42- di chuyển sang cốc đựng dung dịch ZnSO4.
Sự di chuyển của các ion này làm cho các dung dịch muối luôn trung hoà điện.
- Phương trình ion rút gọn biểu diễn quá trình oxi hoá-khử xảy ra trên bề mặt các điện cực của pin điện hoá:
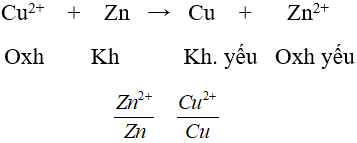
c. Nhận xét
- Có sự biến đổi nồng độ các ion Cu2+ và Zn2+ trong quá trình hoạt động của pin. Cu2+ giảm, Zn2+ tăng
- Năng lượng của phản ứng oxi hóa – khử trong pin điện hóa đã sinh ra dòng điện một chiều.
- Những yếu tố ảnh hưởng đến suất điện động của pin điện hóa như:
+ Nhiệt độ.
+ Nồng độ của ion kim loại.
+ Bản chất của kim loại làm điện cực.
- Trong pin điện hóa:
+ Cực âm (anot): xảy ra quá trình oxi hóa
+ Cực dương (catot): xảy ra quá trình khử
III. Thế điện cực chuẩn của kim loại
1. Điện cực hiđro chuẩn
Trên bề mặt điện cực hiđro xảy ra cân bằng oxi hóa – khử của cặp oxi hóa – khử 2H+/H2
Quy ước rằng: thế điện cực của điện cực hiđro chuẩn bằng 0,00 V ở mọi nhiệt độ, tức là:
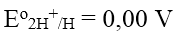
2. Thế điện cực chuẩn của kim loại
Thế điện cực tiêu chuẩn của kim loại cần đoc được chấp nhận bằng bằng suất điện động của pin tạo bởi điện cực hiđro chuẩn và điện cực chuẩn của kim loại cần đo. Có 2 trường hợp xảy ra với giá trị của thế điện cực chuẩn:
- Thế điện cực chuẩn của cặp Mn+/M là số dương nếu khả năng oxi hóa của ion Mn+ trong nửa pin Mn+/M là mạnh hơn ion H+ trong nửa pin 2H+/H2
- Thế điện cực chuẩn của cặp Mn+/M là số âm nếu khả năng oxi hóa của ion Mn+ trong nửa pin Mn+/M là yếu hơn ion H+ trong nửa pin 2H+/H2
Ví dụ: Thế điện cực chuẩn của các cặp kim loại:
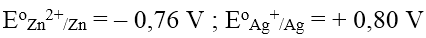
IV. Dãy thế điện cực chuẩn
Dãy thế điện cực chuẩn của kim loại còn được gọi là dãy thế oxi hóa – khử chuẩn của kim loại, hoặc dãy thế khử chuẩn của kim loại.

V. Ý nghĩa của dãy thế điện cực chuẩn của kim loại
1. So sánh tính oxi hóa – khử
Trong dung môi nước, thế điện cực chuẩn của kim loại 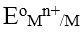
2. Xác định chiều của phản ứng oxi hóa – khử
Xác định chiều của phản ứng oxi hóa – khử cũng là sự tìm hiểu về phản ứng đó trong điều kiện tự nhiên có xảy ra hay không.
3. Xác định suất điện động chuẩn của pin điện hóa
Suất điện động chuẩn của pin điện hóa (E0pin) bằng thế điện cực chuẩn của cực dương trừ đi thế điện cực chuẩn của cực âm. Suất điện động của pin điện hóa luôn là số dương.
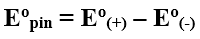
4. Xác định thế điện cực chuẩn của cặp oxi hóa – khử
Ta có thể xác định được thế điện cực chuẩn của cặp oxi hóa – khử khi biết suất điện động chuẩn của pin điện hóa (E0pin) và thế điện cực chuẩn của cặp oxi hóa – khử còn lại.
E0(+) = E0pin + E0(-); E0(-) = E0(+) – E0pin
FIle tải hướng dẫn soạn Hóa 12 Bài 18 trang 88, 89 file DOC:
Hy vọng tài liệu sẽ hữu ích cho các em học sinh và quý thầy cô tham khảo và đối chiếu đáp án chính xác.
►Ngoài ra các em học sinh và thầy cô có thể tham khảo thêm nhiều tài liệu hữu ích hỗ trợ ôn luyện thi môn Hóa như đề kiểm tra, hướng dẫn giải sách giáo khoa, vở bài tập được cập nhật liên tục tại chuyên trang của chúng tôi.
 Báo cáo thực hành Hóa học 12 Bài 24 đầy đủ nhất
Báo cáo thực hành Hóa học 12 Bài 24 đầy đủ nhất Hướng dẫn giải bài 17 Hóa 12 chi tiết và chính xác nhất
Hướng dẫn giải bài 17 Hóa 12 chi tiết và chính xác nhất Giải Hóa 12 Bài 18: Tính chất của kim loại. Dãy điện hóa của kim loại
Giải Hóa 12 Bài 18: Tính chất của kim loại. Dãy điện hóa của kim loại Giải Hoá học 12 Bài 23: Luyện tâp: Điều chế kim loại và sự ăn mòn kim loại trang 103 SGK
Giải Hoá học 12 Bài 23: Luyện tâp: Điều chế kim loại và sự ăn mòn kim loại trang 103 SGK Giải Hoá học 12 Bài 21: Điều chế kim loại trang 98 SGK
Giải Hoá học 12 Bài 21: Điều chế kim loại trang 98 SGK Giải Hoá học 12 Bài 22: Luyện tập: Tính chất của kim loại trang 100, 101 SGK
Giải Hoá học 12 Bài 22: Luyện tập: Tính chất của kim loại trang 100, 101 SGK Giải Hoá học 12 Bài 20: Sự ăn mòn kim loại trang 95 SGK
Giải Hoá học 12 Bài 20: Sự ăn mòn kim loại trang 95 SGK Giải Hoá học 12 Bài 19: Hợp kim trang 91 SGK
Giải Hoá học 12 Bài 19: Hợp kim trang 91 SGK