Giải SBT Hóa học 9 Bài 1: Tính chất hóa học của oxit. Khái quát về sự phân loại oxit (chính xác nhất)
Mời thầy cô và các bạn học sinh tham khảo ngay Giải SBT Hóa 9 Bài 1: Tính chất hóa học của oxit. Khái quát về sự phân loại oxit (ngắn gọn) được đội ngũ chuyên gia biên soạn ngắn gọn và đầy đủ nhất dưới đây.
Giải Hóa học 9 Bài 1 SBT: Tính chất hóa học của oxit. Khái quát về sự phân loại oxit
Bài 1.1 trang 3 Sách bài tập Hóa học 9
Có những oxit sau : H2O, SO2, CuO, CO2, CaO, MgO. Hãy cho biết những chất nào có thể điều chế bằng
a) phản ứng hoá hợp ? Viết phương trình hoá học.
b) phản ứng phân huỷ ? Viết phương trình hoá học
Lời giải:
a) Điều chế bằng phương pháp hoá hợp : H2O, SO2, CuO, CO2, CaO, MgO.
b) Điều chế bằng phương pháp phân huỷ : CuO, CO2, CaO, MgO.
Thí dụ :
CuCO3 to→ CuO + CO2
CaCO3 to→ CaO + CO2
MgCO3 to→ MgO + CO2
Bài 1.2 trang 3 Sách bài tập Hóa học 9
Hãy viết công thức hoá học và tên gọi của
a) 5 oxit bazơ ;
b) 5 oxit axit.
Lời giải:
a) Các oxit bazơ : đồng(II) oxit : CuO, natri oxit : Na2O, canxi oxit : CaO, sắt(III) oxit: Fe2O3 ...
b) Các oxit axit: cacbon đioxit (CO2), lưu huỳnh đioxit (SO2), đinitơ pentaoxit (N2O5) ...
Bài 1.3 trang 3 Sách bài tập Hóa học 9
Khí cacbon monooxit (CO) có lẫn các tạp chất là khí cacbon đioxit (CO2) và lưu huỳnh đioxit (SO2) Làm thế nào tách được những tạp chất ra khỏi CO ? Viết các phương trình hoá học.
Lời giải:
Dẫn hỗn hợp khí qua dung dịch bazơ dư, các tạp chất là oxit axit bị giữ lại. Đi ra khỏi dung dịch là khí CO (oxit trung tính không tác dụng với bazơ).
Phương trình phản ứng
CO2 + Ca(OH)2 → CaCO3 + H2O
SO2 + Ca(OH)2 → CaSO3 + H2O
Bài 1.4 trang 3 Sách bài tập Hóa học 9
Hãy tìm công thức hoá học của những oxit có thành phần khối lượng như sau :
a) S : 50% ; b) C : 42,8% ; c) Mn : 49,6% ; d) Pb : 86,6%.
Lời giải:
a) Đặt công thức hoá học của oxit lưu huỳnh là SxOy, ta có :
x:y = 50/32 : 50/ 16 = 1:2
Oxit của lưu huỳnh có công thức hoá học là SO2.
b) C: 42,8% ⇒ O: 57,2%
Gọi công thức oxit là: CxHy
⇒ x : y = 42,8/12 : 57,2/16 = 1 : 1
Vậy oxit là: CO
c) Mn: 49,6% ⇒ O: 50,4%
Gọi công thức là: MnxOy
x : y = 49,6/55 : 50,4/16 = 2 : 7
Vậy oxit là: Mn2O7
d) Pb: 86,6% ⇒ O: 13,4%
Gọi công thức của oxit là: PbxOy
x : y = 86,6/207 : 13,4/16 = 1 : 2
Vậy công thức oxit là: PbO2
Bài 1.5 trang 3 Sách bài tập Hóa học 9
Biết rằng 1,12 lít khí cacbon đioxit (đktc) tác dụng vừa đủ với 100 ml dung dịch NaOH tạo ra muối trung hoà.
a) Viết phương trình hoá học.
b) Tính nồng độ mol của dung dịch NaOH đã dùng.
Lời giải:
a) CO2 + 2NaOH → Na2CO3 + H2O
b) nNaOH = 2nCO2 = 1,12x2 /22,4 = 0,1 (mol)
Nồng độ mol của dung dịch NaOH là 1M.
Bài 1.6 trang 4 Sách bài tập Hóa học 9
Cho 15,3 gam oxit của kim loại hoá trị II vào nước thu được 200 gam dung dịch bazơ với nồng độ 8,55%. Hãy xác định công thức của oxit trên.
Lời giải:
Cách 1: Đặt công thức hoá học của oxit là MO ⇒ công thức bazơ là M(OH)2
MO + H2O → M(OH)2
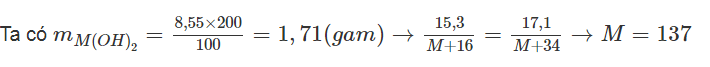
→ Công thức oxit là BaO.
Cách 2: mH2O(p/u) = mM(OH)2 - mMO = 17,1 - 15,3 = 1,8(g)
MO + H2O → M(OH)2
.png)
Công thức oxit là BaO
Bài 1.7 trang 4 Sách bài tập Hóa học 9
Cho 38,4 gam một oxit axit của phi kim X có hoá trị IV tác dụng vừa đủ với dung dịch NaOH thu được 400 gam dung dịch muối nồng độ 18,9%. Xác định công thức của oxit.
Lời giải:
Cách 1 : Đặt công thức của oxit là XO2.
mmuối = 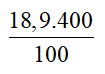 = 75,6 (g)
= 75,6 (g)
XO2 + 2NaOH → Na2XO3 + H2O
Theo phương trình hoá học 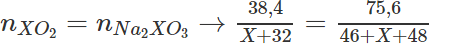
=> X = 32 => Công thức oxit là SO2.
Cách 2: mmuoi = 75,6(g) → mNa2O = 75,6 - 38,4 = 37,2(g)
nNa2O = 37,2/62 = 0,6 (mol)
nXO2 = nNa2O = 0,6 mol
→ MXO2 = 38,4/0,6 = 64(gam/mol)
→ X = 32
=> Công thức oxit là SO2.
►►► CLICK NGAY vào nút TẢI VỀ dưới đây để tải về Giải SBT Hóa học 9 Bài 1: Tính chất hóa học của oxit. Khái quát về sự phân loại oxit (chính xác nhất) file PDF hoàn toàn miễn phí.
 Giải SBT Hóa học 9 Bài 18: Nhôm (chính xác nhất)
Giải SBT Hóa học 9 Bài 18: Nhôm (chính xác nhất) Giải SBT Hóa học 9 Bài 33: Thực hành: Tính chất hóa học của phi kim và hợp chất của chúng (chính xác nhất)
Giải SBT Hóa học 9 Bài 33: Thực hành: Tính chất hóa học của phi kim và hợp chất của chúng (chính xác nhất) Giải SBT Hóa học 9 Bài 25: Tính chất của phi kim (chính xác nhất)
Giải SBT Hóa học 9 Bài 25: Tính chất của phi kim (chính xác nhất) Giải SBT Hóa học 9 Bài 56: Ôn tập cuối năm: Phần 1: Hóa vô cơ (chính xác nhất)
Giải SBT Hóa học 9 Bài 56: Ôn tập cuối năm: Phần 1: Hóa vô cơ (chính xác nhất) Giải SBT Hóa học 9 Bài 55: Thực hành: Tính chất của gluxit (chính xác nhất)
Giải SBT Hóa học 9 Bài 55: Thực hành: Tính chất của gluxit (chính xác nhất) Giải SBT Hóa học 9 Bài 54: Polime (chính xác nhất)
Giải SBT Hóa học 9 Bài 54: Polime (chính xác nhất) Giải SBT Hóa học 9 Bài 53: Protein (chính xác nhất)
Giải SBT Hóa học 9 Bài 53: Protein (chính xác nhất) Giải SBT Hóa học 9 Bài 52: Tinh bột và xenlulozơ (chính xác nhất)
Giải SBT Hóa học 9 Bài 52: Tinh bột và xenlulozơ (chính xác nhất)

