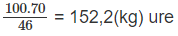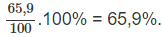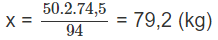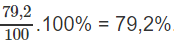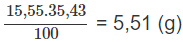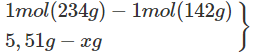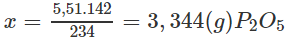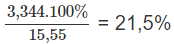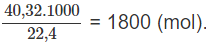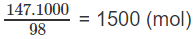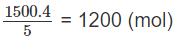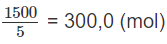Giải SBT Hóa Học 11 Bài 12: Phân bón hóa học (chính xác nhất)
Mời các em học sinh và quý thầy cô tham khảo ngay hướng dẫn Giải SBT Hóa học 11 Bài 12: Phân bón hóa học (chính xác nhất) được đội ngũ chuyên gia biên soạn ngắn gọn và đầy đủ dưới đây.
Giải Hóa học 11 Bài 12 SBT: Phân bón hóa học
Bài 12.1 trang 19 sách bài tập Hóa 11
Phân đạm urê thường chỉ chứa 46,00% N. Khối lượng (kg) urê đủ để cung cấp 70,00 kg N là
A. 152,2.
B. 145,5.
C. 160,9.
D. 200,0.
Lời giải:
Đáp án: A.
46,00 kg N có trong 100 (kg) ure
70,00 kg N có trong
Bài 12.2 trang 19 sách bài tập Hóa 11
Phân supephotphat kép thực tế sản xuất được thường chỉ ứng với 40,0% P2O5. Hàm lượng (%) của canxi đihiđrophotphat trong phân bón này là
A. 69,0.
B. 65,9.
C. 71,3.
D. 73,1.
Lời giải:
Đáp án: B.
Trong 100 kg phân supephotphat kép có 40 kg P2O5. Khối lượng Ca(H2PO4)2 tương ứng với khối lượng P2O5 trên được tính theo tỉ lệ :
P2O5 - Ca(H2PO4)2
142 g 234 g
40 kg x kg
Hàm lượng (%) của Ca(H2PO4)2:
Bài 12.3 trang 19 sách bài tập Hóa 11
Phân kali clorua sản xuất được từ quặng xinvinit thường chỉ ứng với 50,00% K2O. Hàm lượng (%) của KCl trong phân bón đó là
A. 72,9.
B. 76,0.
C. 79,2.
D. 75,5.
Lời giải:
Đáp án: C.
Cứ 100 kg phân bón thì có 50 kg K2O.
Khối lượng phân bón KCl tương ứng với 50 kg K2O được tính theo tỉ lệ
K2O - 2KCl
94 g 2 x 74,5 g
50 kg x kg ;
Hàm lương (%) của KCl :
Bài 12.4 trang 19 sách bài tập Hóa 11
Từ amoniac, đá vôi, nước, không khí, chất xúc tác thích hợp hãy viết phương trình hoá học của các phản ứng điều chế phân đạm :
1. canxi nitrat;
2. amoni nitrat.
Lời giải:
2NO + O2 → 2NO2
4NO2 + 2H2O + O2 → 4HNO3
1. Điều chế canxi nitrat :
2HNO3 + CaCO3 → Ca(NO3)2 + CO2 + H2O
2. Điều chế amoni nitrat :
HNO3 + NH3 → NH4NO3
Bài 12.5 trang 19 sách bài tập Hóa 11
Viết phương trình hoá học thực hiện dãy chuyển hoá sau :
Bột photphorit (1)→ axit photphoric (2)→ amophot (3)→ canxiphotphat (4)→ axit photphoric (5)→ supephotphat kép.
Lời giải:
Các phương trình hoá học thực hiện dãy chuyển hoá :
(1) Ca3(PO4)2 + 3H2SO4(đặc) → 2H3PO4 + 3CaSO4↓
(2) 3NH3 + 2H3PO4 → NH4H2PO4 + (NH4)2HPO4 amophot
(3) NH4H2PO4 + (NH4)2HPO4 + 3Ca(OH)2 dư → Ca3(PO4)2 + 3NH3 + 6H2O
(4) Ca3(PO4)2 + 3SiO2 + 5Cto→ 2P + 3CaSiO3 + 5CO
P + 5HNO3(đặc) → H3PO4 + 5NO2 + H2O
(5) Ca3(PO4)2 + 4H3PO4 → 3Ca(H2PO4)2
Bài 12.6 trang 19 sách bài tập Hóa 11
Một mẫu supephotphat đơn khối lượng 15,55 g chứa 35,43% Ca(H2PO4)2, còn lại là CaSO4. Tính tỉ lệ % P2O5 trong mẫu supephotphat đơn trên.
Lời giải:
Khối lượng Ca(H2PO4)2 trong 15,55 g supephotphat đơn:
Khối lượng P2O5 trong mẫu supephotphat đơn trên :
1 Ca(H2PO4)2 - 1 P2O5
% về khối lượng của P2O5:
Bài 12.7 trang 19 sách bài tập Hóa 11
Cho 40,32 m3 amoniac (đktc) tác dụng với 147,0 kg axit photphoric tạo thành một loại phân bón amophot có tỉ lệ số mol
nNH4H2PO4 : n(NH4)2HPO4 = 4 : 1
1. Viết phương trình hoá học của phản ứng tạo thành phân bón amophot đó.
2. Tính khối lượng (kg) của amophot thu được.
Lời giải:
1. Phương trình hoá học tạo thành loại phân bón amophot phù hợp với đề bài :
6NH3 + 5H3PO4 → 4NH4H2PO4 + (NH4)2HPO4 (1)
2. Tính khối lượng amophot thu được :
Số mol NH3:
Số mol H3PO4:
Tỉ lệ số mol NH3: số mol H3PO4 = 1800 : 1500 = 6:5, vừa đúng bằng tỉ lệ hợp thức trong phương trình hoá học (1). Vậy lượng NH3 phản ứng vừa đủ với lượng H3PO4. Do đó, có thể tính lượng chất sản phẩm thec NH3 hoặc theo H3PO4.
Theo lượng H3PO4, số mol NH4H2PO4:
và số mol (NH4)2HPO4:
Khối lượng amophot thu được:
mNH4H2PO4 + m(NH4)2HPO4 = 1200.115 + 300.132 = 177,6.103 (g) hay 177,6 kg
►►CLICK NGAY vào nút TẢI VỀ dưới đây để tải về Giải SBT Hóa 11 Bài 12: Phân bón hóa học (ngắn gọn nhất) file PDF hoàn toàn miễn phí.
 Giải SBT Hóa Học 11 Bài 45: Axit cacboxylic (chính xác nhất)
Giải SBT Hóa Học 11 Bài 45: Axit cacboxylic (chính xác nhất) Giải SBT Hóa Học 11 Bài 41: Phenol (chính xác nhất)
Giải SBT Hóa Học 11 Bài 41: Phenol (chính xác nhất) Giải SBT Hóa Học 11 Bài 40: Ancol (chính xác nhất)
Giải SBT Hóa Học 11 Bài 40: Ancol (chính xác nhất) Giải SBT Hóa Học 11 Bài 36: Luyện tập: Hiđrocacbon thơm (chính xác nhất)
Giải SBT Hóa Học 11 Bài 36: Luyện tập: Hiđrocacbon thơm (chính xác nhất) Giải SBT Hóa Học 11 Bài 33: Luyện tập: Ankin (chính xác nhất)
Giải SBT Hóa Học 11 Bài 33: Luyện tập: Ankin (chính xác nhất) Giải SBT Hóa Học 11 Bài 31: Luyện tập: Anken và ankađien (chính xác nhất)
Giải SBT Hóa Học 11 Bài 31: Luyện tập: Anken và ankađien (chính xác nhất) Giải SBT Hóa Học 11 Bài 44: Anđehit - Xeton (chính xác nhất)
Giải SBT Hóa Học 11 Bài 44: Anđehit - Xeton (chính xác nhất) Giải SBT Hóa Học 11 Bài 42: Luyện tập: Dẫn xuất halogen, ancol, phenol
Giải SBT Hóa Học 11 Bài 42: Luyện tập: Dẫn xuất halogen, ancol, phenol