Giải Hoá 9 Bài 19: Sắt SGK trang 60 (chính xác nhât)
Sau bài học các em sẽ được nghiên cứu về tính chất vật lý, tính chất hóa học và các kiến thức liên quan đến Sắt. Từ đó vận dụng kiến thức đã học để giải các bài tập ứng dụng và chứng minh các hiện tượng thực tiễn trong cuộc sống có liên quan.
Giải bài tập SGK Hóa 9 Bài 19
Giải Bài 1 trang 60 SGK Hoá 9
Sắt có những tính chất hóa học nào ? Viết các phương trình hóa học minh họa.
Lời giải:
a) Tác dụng với phi kim :
Tác dụng với oxi : 3Fe + 2O2 → Fe3O4(to)
Tác dụng với clo : 2Fe + 3Cl2 → 2FeCl3(to)
Lưu ý: Fe tác dụng với clo chỉ cho Fe (III) clorua (không cho Fe(II) clorua).
b) Tác dụng với dung dịch axit: Sắt tác dụng với dung dịch HCl, H2SO4 loãng cho muối sắt (II) và giải phóng H2.
Fe + 2HCl → FeCl2 + H2 ↑
Lưu ý: Fe tác dụng với dung dịch HCl chỉ cho Fe (II) clorua (không cho Fe(III) clorua).
Fe không tác dụng với HNO3 đặc, nguội và H2SO4 đặc, nguội.
c) Tác dụng với dung dịch muối:
Fe + CuSO4 → FeSO4 + Cu
Sắt tác dụng với dung dịch muối sắt (II) và giải phóng kim loại mới.
Giải bài 2 Hoá 9 SGK trang 60
Từ sắt và các hóa chất cần thiết, hãy viết các phương trình hóa học để thu được các oxit riêng biệt: Fe3O4, Fe2O3 và ghi rõ điều kiện phản ứng, nếu có:
Lời giải:
Các PTHH:
∗ Fe3O4
3Fe + 2O2 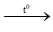 Fe3O4
Fe3O4
∗ Fe2O3
Sơ đồ: Fe + Cl2→ FeCl3 + NaOH→ Fe(OH)3 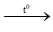 Fe2O3
Fe2O3
2Fe + 3Cl2 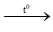 2FeCl3
2FeCl3
FeCl3 + 3NaOH → Fe(OH)3 + 3NaCl
2Fe(OH)3 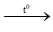 Fe2O3 + 3H2O
Fe2O3 + 3H2O
Giải bài 3 SGK Hoá 9 trang 60
Có bột kim loại sắt lẫn tạp chất nhôm. Hãy trình bày phương pháp làm sạch sắt.
Lời giải:
Cho bột kim loại sắt có lẫn nhôm vào dung dịch NaOH dư, chỉ có nhôm phản ứng, sắt sẽ không phản ứng
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2 ↑
Sau khi khí bay ra hết, tức nhôm đã phản ứng hết, lọc dung dịch sau phản ứng thấy còn chất rắn không tan, đó là sắt.
Giải Bài 4 trang 60 SGK Hoá 9
Sắt tác dụng được với chất nào sau đây?
a) Dung dịch muối Cu(NO3)2
b) H2SO4 đặc, nguội
c) Khí Cl2
d) Dung dịch ZnSO4.
Viết các phương trình hóa học và ghi điều kiện, nếu có:
Lời giải:
Sắt tác dụng với dung dịch muối Cu(NO3)2 (a) và khí Cl2 (c):
Fe + Cu(NO3)2 → Fe(NO3)2 + Cu ↓
(kim loại mạnh đẩy kim loại yếu ra khỏi dung dịch muối)
2Fe + 3Cl2 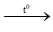 2FeCl3.
2FeCl3.
Lưu ý: Sắt bị thụ động hóa trong môi trường H2SO4 đặc nguội và HNO3 đặc nguội.
Giải Bài 5 Hoá 9 SGK trang 60
Ngâm bột sắt dư trong 10ml dung dịch đồng sunfat 1M. Sau khi phản ứng kết thúc, lọc được chất rắn A và dung dịch B.
a) Cho A tác dụng với dung dịch HCl dư. Tính khối lượng chất rắn còn lại sau phản ứng.
b) Tính thể tích dung dịch NaOH 1M vừa đủ để kết tủa hoàn toàn dung dịch B.
Lời giải:
a) nCuSO4 = CM .V = 1. 0,01 = 0,01 (mol)
PTHH: Fe + CuSO4 → FeSO4 + Cu (1)
Chất rắn A gồm sắt dư và đồng, dung dịch B là FeSO4.
nCu = nCuSO4 = 0,01 mol
PTHH cho A + dd HCl:
Fe + 2HCl → FeCl2 + H2 ↑ (2)
Cu + HCl → không phản ứng.
Khối lượng chất rắn còn lại sau phản ứng với HCl chỉ có Cu
mCu = 0,01 x 64 = 0,64g.
b) Dung dịch B chỉ có FeSO4:
FeSO4 + 2NaOH → Fe(OH)2 ↓ + Na2SO4 ( 3)
Theo pt (1) nFeSO4 = nCuSO4 = 0,01 mol
Theo pt (3) nNaOH = 2. nFeSO4 = 2. 0,01 = 0,02 mol
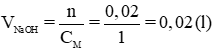
Lý thuyết trọng tâm Hóa 9 Bài 19: Sắt
I. Tính chất vật lí:
Sắt là kim loại màu trắng xám, khi ở dạng bột có màu đen.
Sắt có tính nhiễm từ (bị nam châm hút và sắt cũng có thể nhiễm từ trở thành nam châm). Khối lượng riêng D = 7,86g/cm3, nóng chảy ở 1539°C.
Sắt dẻo nên dễ rèn.
II. Tính chất hóa học:
Sắt có những tính chất hóa học của kim loại
1. Tác dụng với nhiều phi kim
Sắt tác dụng với oxi tạo thành oxit, tác dụng với nhiều phi kim tạo thành muối.
Ví dụ:
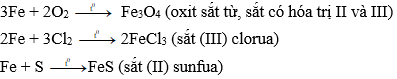
2. Tác dụng với dung dịch axit
Sắt tác dụng với dung dịch axit HCl và H2SO4 loãng tạo thành muối sắt (II) và giải phóng H2.
Phương trình hóa học:
Fe + 2HCl → FeCl2 + H2
Fe + H2SO4 → FeSO4 + H2
Chú ý: Sắt không tác dụng với HNO3 đặc, nguội và H2SO4 đặc, nguội.
Khi sắt phản ứng với HNO3 loãng, H2SO4 đặc, nóng sản phẩm thu được chứa muối sắt (III) và không giải phóng H2.
3. Tác dụng với dung dịch muối của kim loại yếu hơn
Ví dụ:
Fe + CuSO4 → FeSO4 + Cu
►►► CLICK NGAY vào nút TẢI VỀ dưới đây để tải về Giải bài tập Hóa 9 Bài 19: Sắt SGK trang 60 file PDF hoàn toàn miễn phí!
 Hóa 9: Bài 23: Báo cáo thực hành tính chất hóa học của nhôm và sắt
Hóa 9: Bài 23: Báo cáo thực hành tính chất hóa học của nhôm và sắt Soạn Hóa Lớp 9 Bài 15: Tính chất vật lý của kim loại đầy đủ nhất
Soạn Hóa Lớp 9 Bài 15: Tính chất vật lý của kim loại đầy đủ nhất Soạn Hóa Lớp 9 Bài 17: Dãy hoạt động hóa học của kim loại đầy đủ nhất
Soạn Hóa Lớp 9 Bài 17: Dãy hoạt động hóa học của kim loại đầy đủ nhất Giải Hoá học 9 Bài 20: Hợp kim sắt: Gang thép trang 63 SGK
Giải Hoá học 9 Bài 20: Hợp kim sắt: Gang thép trang 63 SGK Soạn Hóa học Lớp 9 Bài 16: Tính chất hóa học của kim loại
Soạn Hóa học Lớp 9 Bài 16: Tính chất hóa học của kim loại Giải Hoá học 9 Bài 22: Luyện tập chương 2: Kim loại trang 69 SGK
Giải Hoá học 9 Bài 22: Luyện tập chương 2: Kim loại trang 69 SGK Giải Hoá 9 Bài 19: Sắt SGK trang 60 (chính xác nhât)
Giải Hoá 9 Bài 19: Sắt SGK trang 60 (chính xác nhât) Soạn Hóa học Lớp 9 Bài 18: Nhôm đầy đủ nhất
Soạn Hóa học Lớp 9 Bài 18: Nhôm đầy đủ nhất

