Soạn Hóa lớp 11 Bài 20: Mở đầu về hóa học hữu cơ
Để quá trình tiếp thu kiến thức mới trở nên dễ dàng và đạt hiệu quả nhất, trước khi bắt đầu bài học mới các em cần có sự chuẩn bị nhất định qua việc tổng hợp nội dung kiến thức lý thuyết trọng tâm, sử dụng những kiến thức hiện có thử áp dụng giải các bài tập ứng dụng, trả lời câu hỏi liên quan. Dưới đây chúng tôi đã soạn sẵn Lời giải Bài 20: Mở đầu về hóa học hữu cơ đầy đủ nhất, giúp các em tiết kiệm thời gian. Nội dung chi tiết được chia sẻ dưới đây.
Bài 20: Mở đầu về hóa học hữu cơ
Bài tập ứng dụng:
Bài 1 (trang 91 SGK Hóa 11):
So sánh hợp chất vô cơ và hợp chất hữu cơ về: thành phần nguyên tố, đặc điểm liên kết hoá học trong phân tử.
Hướng dẫn giải chi tiết:
Thành phần nguyên tố:
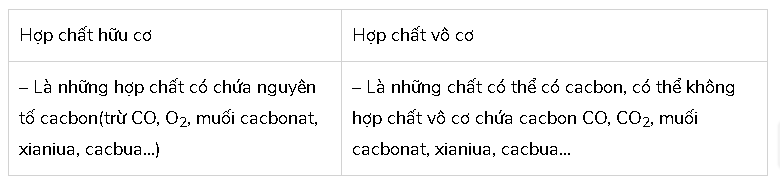
Đặc điểm liên kết hoá học trong phân tử:

Bài 2 (trang 91 SGK Hóa 11):
Nếu mục đích và phương pháp tiến hành phân tích định tính và định lượng nguyên tố.
Hướng dẫn giải chi tiết:
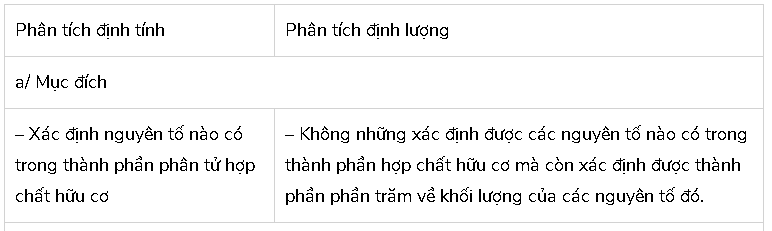
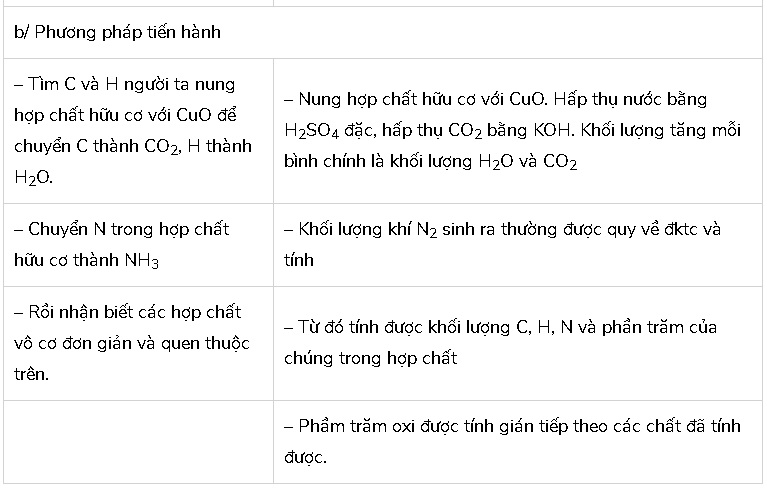
Bài 3 (trang 91 SGK Hóa 11):
Oxi hoá hoàn toàn 0,6 gam hợp chất hữu cơ A thu được 0,672 lít CO2 (đktc) và 0,72 gam H2O. Tính thành phần phần trăm khối lượng của các nguyên tố trong phân tử chất A.
Hướng dẫn giải chi tiết:
Gọi CTPT của hợp chất hữu cơ là CxHyOz (x, y, z nguyên dương; z ≥ 0)
Ta có:
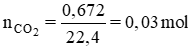
BT nguyên tố ⇒ nC = nCO2 = 0,03 mol ⇒ mC = 12. 0,03 = 0,36g
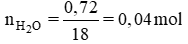
BT nguyên tố ⇒ nH = 2.nH2O = 2. 0,04 = 0,08 mol ⇒ mH = 0,08. 1 = 0,08 g
mO = 0,6 - 0,36 - 0,08 = 0,16(g)
⇒ Hợp chất A có chứa C, H, O
Phần trăm khối lượng các nguyên tố trong phân tử A là:

Bài 4 (trang 91 SGK Hóa 11):
β-Caroten (chất hữu cơ có trong củ cà rốt) có màu da cam. Nhờ tác dụng của enzim ruốt non,β-Croten chuyển thành vitamin A nên nó còn được gọi là tiến vitamin A. Oxi hoá hoàn toàn 0,67 gam β-Caroten rồi dẫn sản pẩm oxi hoá qua bình (1) đựng dung dịch H2SO4 đặc, sau đó qua bình (2) đựng dung dịch Ca(OH)2 dư. Kết quả cho thấy khối lượng bình (1) tăng 0,63 gam; bình (2) có 5 gam kết tủa. Tính phần trăm khối lượng của các nguyên tố trong phân tử β-Caroten
Hướng dẫn giải chi tiết:
Ca(OH)2 + CO2 → CaCO3 + H2O
Khối lượng bình (1) tăng là khối lượng của H2O = 0,63(g)
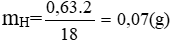
mCaCO3 = 5g ⇒ nCO2 = nCaCO3 = 5/100 = 0,05 mol
BT nguyên tố ⇒ nC = nCO2 = 0,05 mol ⇒ mC = 12. 0,05 = 0,6 g
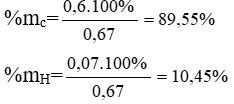
%mO = 100% - (89,55 + 10,45)% = 0%
Lý thuyết trọng tâm:
I. Hợp chất hữu cơ và hóa học hữu cơ
1. Khái niệm
- Hợp chất hữu cơ là các hợp chất của C trừ oxit của C, muối cacbua, muối cacbonat, muối xianua.
- Hoá học hữu cơ là ngành hóa học chuyên nghiên cứu các hợp chất hữu cơ.
2. Phân loại hợp chất hữu cơ.
Hợp chất hữu cơ được chia thành hidrcacbon và dẫn xuất hidrcacbon.
a/ Hidrcacbon là loại hợp chất hữu cơ đơn giản nhất, trong thành phần phân tử chỉ chứa hai nguyên tố là cacbon và hidro.
- Hidrocacbon mạch hở:
+ Hidrocacbon no: Ankan CH4
+ Hidrocacbon không no có một nối đôi: Anken C2H4
+ Hidrcacbon không no có hai nối đôi: Ankadien
- Hidrocacbon mạch vòng:
+ Hidrocacbon no: xicloankan
+ Hidrocacbon mạch vòng: Aren
b/ Dẫn xuất của hidrocacbon là những hợp chất mà trong phân tử ngoài C, H ra còn có một số hay nhiều nguyên tố khác như O, N, S, halogen...
- Dẫn xuất halogen: R – X ( R là gốc hidrocacbon)
- Hợp chất chứa nhóm chức:
- OH - : ancol; - O - : ete; - COOH: axit......
3/ Đặc điểm chung
- Hợp chất hữu cơ nhất thiết phải chứa C, hay có H thường gặp O ngoài ra còn có halogen, N, P...
- Liên kết chủ yếu trong hợp chất hữu cơ là liên kết cộng hóa trị.
- Các hợp chất hữu cơ thường dễ bay hơi, dễ cháy, kém bền nhiệt.
- Các phản ứng trong hoá học hữu cơ thường chậm, không hoàn toàn, xảy ra theo nhiều hướng thường phải đun nóng và có xúc tác.
4/ Các phương pháp tinh chế hợp chất hữu cơ
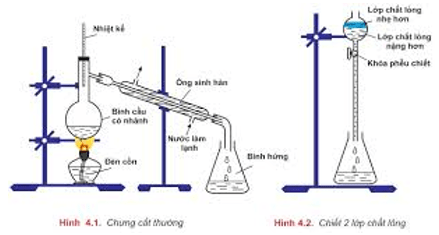
- Chưng cất: để tách các chất lỏng có nhiệt độ sôi khác nhau nhiều.
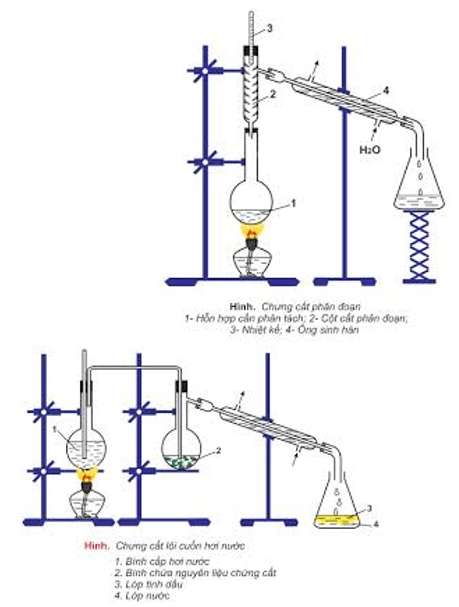
- Chiết: để tách hai chất lỏng không trộn lẫn vào nhau.
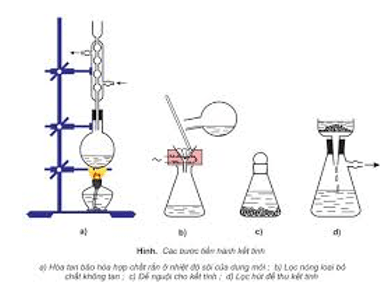
- Kết tinh lại: để tách các chất rắn có độ tan khác nhau theo nhiệt độ.
II. Phân tích nguyên tố
Để xác định công thức phân tử hợp chất hữu cơ người ta phải xác định :
- Thành phần định tính nguyên tố.
- Thành phần định lượng nguyên tố.
- Xác định khối lượng phân tử.
1. Phân tích định tính nguyên tố.
- Phân tích định tính nguyên tố để xác định thành phần các nguyên tố hóa học chứa trong một chất.
- Muốn xác định thành phần các nguyên tố , người ta chuyển các nguyên tồ trong hợp chất hữu cơ thành các hợp chất vô cơ đơn giản rồi nhận ra các sản phẩm đó.
a. Xác định cacbon và hidro.
- Nhận Cacbon: Đốt cháy hợp chất hữu cơ:
C −+O2→ CO2 −+Ca(OH)2→ CaCO3
- Nhận Hidro: Đốt cháy hợp chất hữu cơ:
2H −+O2→ H2O −+CuSO4 khan→ CuSO4.5H2O ( màu xanh lam)
- Hoặc có thể dùng chất hút nước mạnh như : H2SO4 đđ, CaCl2 khan, P2O5.
b. Xác định nitơ và oxi.
- Nhận N: Đốt cháy hợp chất hữu cơ, nếu có mùi khét thì hợp chất đó có nitơ.
Hoặc đun hợp chất hữu cơ với H2SO4 đặc ( NaOH đặc) có mùi khai NH3 thì hợp chất đó có chứa nitơ.
CxHyOzNt −+ H2SO4đ, tº→ (NH4)2SO4+......
(NH4)2SO4 + 2NaOH −tº→ Na2SO4 + H2O + NH3↑
- Nhận O : Khó phân tích định tính trực tiếp, thường xác định nhờ định lượng:
mO = mhợp chất – tổng khối lượng các nguyên tố
c. Xác định halogen.
Khi đốt cháy hợp chất hữu cơ chứa clo bị phân hủy, clo tách ra dưới dạng HCl, ta dùng dung dịch AgNO3
HCl + AgNO3 → AgCl↓ + HNO3
2. Phân tích định lượng các nguyên tố:
- Phân tích định lượng các nguyên tố xác định khối lượng của mỗi nguyên tố hóa học chứa trong hợp chất hữu cơ.
- Muốn định lượng nguyên tố, người ta chuyển các nguyên tố trong hợp chất hữu cơ thành các hợp chất vô cơ đơn giản, định lượng chúng, từ đó suy ra khối lượng từng nguyên tố có trong một chất.
a. Định lượng cacbon và hidro.
VD: Đốt cháy chất hữu cơ A thu được CO2 và H2O và N2
mC (A) = mC(CO2) = nCO2.12
mH(A) = mH(H2O) = nH2O.2
b. Định lượng nitơ
mN(A) = nN2.28
c. Định lượng oxi
mO = m(A) – ( mC + mH + mN ).
* Chú ý :
- Dùng H2SO4 đặc, P2O5, CaCl2 khan hấp thụ H2O.
- Dùng NaOH, KOH, Ca(OH)2 hấp thụ CO2, độ tăng khối lượng của bình hay khối lượng kết tủa CaCO3 giúp ta tính được CO2
- Chỉ dùng CaO, Ca(OH)2, NaOH hấp thụ sản phẩm gồm CO2 và H2O thì khối lượng bình tăng chính là tổng khối lượng CO2 và H2O.
3. Thành phần nguyên tố:
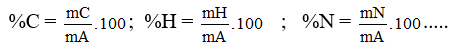
File tải miễn phí soạn - Bài 20: Mở đầu về hóa học hữu cơ Hóa 11:
Hy vọng tài liệu sẽ hữu ích cho các em học sinh và quý thầy cô tham khảo và đối chiếu đáp án chính xác.
►Ngoài ra các em học sinh và thầy cô có thể tham khảo thêm nhiều tài liệu hữu ích hỗ trợ ôn luyện thi môn hóa như đề kiểm tra, hướng dẫn giải sách giáo khoa, vở bài tập được cập nhật liên tục tại chuyên trang của chúng tôi.
 Giải bài tập Hóa 11: Công thức phân tử hợp chất hữu cơ trang 95 đầy đủ
Giải bài tập Hóa 11: Công thức phân tử hợp chất hữu cơ trang 95 đầy đủ Giải bài 24 Hóa học 11: Luyện tập trang 107, 108 chi tiết nhất
Giải bài 24 Hóa học 11: Luyện tập trang 107, 108 chi tiết nhất Soạn Hóa lớp 11 Bài 20: Mở đầu về hóa học hữu cơ
Soạn Hóa lớp 11 Bài 20: Mở đầu về hóa học hữu cơ Giải Hoá học 11 Bài 22: Cấu trúc phân tử hợp chất hữu cơ trang 101, 102 SGK
Giải Hoá học 11 Bài 22: Cấu trúc phân tử hợp chất hữu cơ trang 101, 102 SGK Giải Hoá học 11 Bài 23: Phản ứng hữu cơ trang 105 SGK
Giải Hoá học 11 Bài 23: Phản ứng hữu cơ trang 105 SGK

