Giải Hoá học 11 Bài 5: Luyện tập trang 22, 23 SGK
Giải Hoá học 11 Bài 5: Luyện tập trang 22, 23 SGK giúp các em ôn tập sâu kiến thức thông qua hướng dẫn giải bài tập trong sách giáo khoa bằng các phương pháp giải hay, ngắn gọn. Hỗ trợ các em học tập tốt môn Hoá lớp 11.
Giải bài tập SGK Hóa 11 Bài 5
Giải bài 1 trang 22 SGK Hóa 11
Viết phương trình điện li của các chất sau: K2S, Na2HPO4, NaH2PO4, Pb(OH)2, HBrO, HF, HClO4.
Lời giải:
a. K2S → 2K+ + S2-
b. Na2HPO4 → 2Na+ + HPO42-
HPO42- ⇆ H+ + PO43-
c. NaH2PO4 → Na+ + H2PO4-
H2PO4- ⇆ H+ + HPO42-
HPO42- ⇆ H+ + PO43-
d. Pb(OH)2 ⇆ Pb2+ + 2OH-
Hoặc H2PbO2 ⇆ 2H+ + PbO22-
e. HBrO ⇆ H+ + BrO-
g. HF ⇆ H+ + F-
h. HClO4 ⇆ H+ + ClO4-
Giải bài 2 SGK Hóa 11 trang 22
Một dung dịch có [H+] = 0,010 M. Tính [OH-] và pH của dung dịch. Môi trường của dung dịch này là axit, trung tính hay kiềm? Hãy cho biết màu của quỳ trong dung dịch này?
Lời giải:
[H+] = 0,010M = 10-2M ⇒ pH = -log[H+] = -log(1,0.10-2) = 2
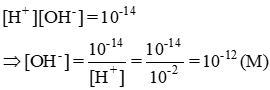
Môi trường của dung dịch này là axit (pH < 7)
Cho quỳ tím vào dung dịch này quỳ sẽ chuyển thành màu đỏ
Giải bài 3 SGK trang 22 Hóa 11
Một dung dịch có pH = 9,0. Tính nồng độ mol của H+ và OH- trong dung dịch? Hãy cho biết màu của phenolphtalein trong dung dịch này?
Lời giải:
pH = 9,0 ≥ [H+] = 10-9 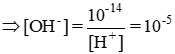
Cho phenolphtalein trong dung dịch này sẽ thấy phenolphtalein chuyển thành màu hồng (khi pH ≥ 8,3 phenolphtalein đổi màu)
Giải bài 4 trang 22 Hóa 11 SGK
Viết phương trình phân tử và ion rút gọn của các phản ứng (nếu có) xảy ra trong dung dịch các cặp chất sau:
a. Na2CO3 + Ca(NO3)2
b. FeSO4 + NaOH (loãng)
c. NaHCO3 + HCl
d. NaHCO3+ NaOH
e. K2CO3 + NaCl
g. Pb(OH)2(r) + HNO3
h. Pb(OH)2(r) + NaOH
i. CuSO4 + Na2S
Lời giải:
a. Na2CO3 + Ca(NO3)2 → 2NaNO3 + CaCO3
Ca2+ + CO32- → CaCO3↓
b. FeSO4 + 2NaOH (loãng) → Fe(OH)2↓ + Na2SO4
Fe2+ + 2OH- → Fe(OH)2↓
c. NaHCO3 + HCl → NaCl + H2O + CO2↑
H+ + HCO3- → H2O + CO2↑
d. NaHCO3 + NaOH → Na2CO3 + H2O
HCO3- + OH- → CO32- + H2O
e. K2CO3 + NaCl Không có phản ứng
g. Pb(OH)2 (r) + 2HNO3 → Pb(NO3)2 + 2H2O
Pb(OH)2 (r) + 2H+ Pb2+ + 2H2O
h. Pb(OH)2 (r) + 2NaOH → Na2PbO2 + 2H2O
Pb(OH)2 (r) + 2OH- → PbO22- + 2H2O
i. CuSO4 + Na2S → CuS + Na2SO4
Cu2+ + S2- → CuS
Giải bài 5 Hóa 11 SGK trang 23
Phản ứng trao đổi ion trong dung dịch chất điện li chỉ xảy ra khi:
A. Các chất phản ứng phải là những chất dễ tan.
B. Các chất phản ứng phải là những chất điện li mạnh.
C. Một số ion trong dung dịch kết hợp được với nhau làm giảm nồng độ ion của chúng.
D. Phản ứng không phải là thuận nghịch.
Hãy chọn câu trả lời đúng.
Lời giải:
Đáp án C
Giải bài 6 Hóa lớp 11 SGK trang 23
Kết tủa CdS được tạo thành bằng dung dịch các cặp chất nào dưới đây:
A. CdCl2 + NaOH
B. Cd(NO3)2 + H2S
C. Cd(NO3)2 + HCl
D. CdCl2 + Na2SO4
Lời giải:
- Đáp án B
Cd(NO3)2 + H2S → CdS↓ + 2HNO3
Giải bài 7 Hóa lớp 11 trang 23 SGK
Viết phương trình hoá học (dưới dạng phân tử và ion rút gọn) của phản ứng trao đổi ion trong dung dịch tạo thành từng chất kết tủa sau:Cr(OH)3 ; Al(OH)3; Ni(OH)2
Lời giải:
CrCl3 + 3NaOH (đủ) → Cr(OH)3 ↓ + 3 NaCl
Cr3+ + 3OH- → Cr(OH)3 ↓
AlCl3 + 3NaOH (đủ) Al(OH)3 ↓ + 3 NaCl
Al3+ + 3OH- → Al(OH)3 ↓
Hoặc AlCl3 + 3NH3 (dư) + 3H2O → Al(OH)3 ↓ + 3NH4Cl
Al3+ + 3NH3 (dư) + 3H2O → Al(OH)3 ↓ + 3NH4+
Ni(NO3)2 + 2NaOH → Ni(OH)2 ↓ + 2NaNO3
Ni2+ + 2OH- → Ni(OH)2 ↓
Lý thuyết Hóa 11 Bài 5: Luyện tập
1. Axit - Bazơ
- Theo A-re-ni-ut:
+ Axit là chất tan trong nước phân li ra ion H+.
+ Bazo khi tan trong nước phân li ra ion OH-.
- Theo Bron-stet:
+ Axit là chất nhường proton H+.
+ Bazo là chất nhận proton H+.
2. Chất lưỡng tính
Là chất vừa thể hiện tính axit, vừa thể hiện tính bazơ.
Ví dụ:
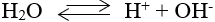
3. Hằng số phân li
Ka là đại lượng đặc trưng cho lực axit của axit yếu trong nước.
Kb là đại lượng đặc trưng cho lực bazo của bazo yếu trong nước.
4. Tích số ion của nước
KH2O = [H+].[OH-] = 10-14 M.
5. Ý nghĩa giá trị [H+] và pH

►►CLICK NGAY vào nút TẢI VỀ dưới đây để tải về Giải Hoá học 11 Bài 5: Luyện tập trang 22, 23 SGK file PDF hoàn toàn miễn phí!
 Giải Hoá học 11 Bài 4: Phản ứng trao đổi ion trong dung dịch các chất điện li trang 20 SGK
Giải Hoá học 11 Bài 4: Phản ứng trao đổi ion trong dung dịch các chất điện li trang 20 SGK Giải Hoá học 11 Bài 6: Bài thực hành 1 trang 24 SGK
Giải Hoá học 11 Bài 6: Bài thực hành 1 trang 24 SGK Giải Hoá học 11 Bài 5: Luyện tập trang 22, 23 SGK
Giải Hoá học 11 Bài 5: Luyện tập trang 22, 23 SGK Giải Hoá học 11 Bài 3: Sự điện li của nước. pH. Chất chỉ thị axit - bazơ trang 14 SGK
Giải Hoá học 11 Bài 3: Sự điện li của nước. pH. Chất chỉ thị axit - bazơ trang 14 SGK Giải Hoá học 11 Bài 2: Axit, bazơ và muối trang 10 SGK
Giải Hoá học 11 Bài 2: Axit, bazơ và muối trang 10 SGK Giải Hoá học 11 Bài 1: Sự điện li trang 7 SGK
Giải Hoá học 11 Bài 1: Sự điện li trang 7 SGK

