Giải Hoá học 11 Bài 29: Anken trang 132 SGK
Giải Hoá học 11 Bài 29: Anken trang 132 SGK giúp các em ôn tập sâu kiến thức thông qua hướng dẫn giải bài tập trong sách giáo khoa bằng các phương pháp giải hay, ngắn gọn. Hỗ trợ các em học tập tốt môn Hoá lớp 11.
Giải bài tập SGK Hóa 11 Bài 29
Giải bài 1 trang 132 SGK Hóa 11
So sánh anken với ankan về đặc điểm cấu tạo và tính chất hóa học. Cho thí dụ minh họa.
Lời giải:
- Về đặc điểm cấu tạo: Khác với ankan là phân tử chỉ chứa liên kết σ, phân tử anken còn có chứa 1 liên kết π kém bền, dễ gẫy.
- Do đó về tính chất hóa học cũng không giống với ankan là cho phản ứng thế là phản ứng đặc trưng, anken cho phản ứng cộng là phản ứng đặc trưng
Ví dụ:
C2H4 + H2→C2H6 (xúc tác : Ni)
C2H4 + Br2→C2H4Br2
C2H4 + HBr→C2H5Br
Ngoài ra anken còn cho phản ứng trùng hợp phản ứng làm mất màu dung dịch thuốc tím.
Ví dụ :
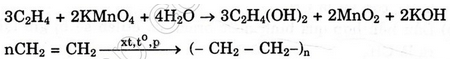
Giải bài 2 SGK Hóa 11 trang 132
Ứng với công thức C5H10 có bao nhiêu đồng phân cấu tạo ?
A. 4 ; B. 5 ; C. 3 ; D. 7
Lời giải:
- Đáp án B
- Các công thức cấu tạo:
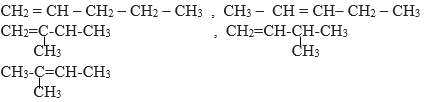
Giải bài 3 SGK trang 132 Hóa 11
Viết phương trình hóa học của phản ứng xảy ra khi:
a. Propilen tác dụng với hidro, đun nóng (xúc tác Ni).
b. But-2-en tác dụng với hirdo clorua.
c. Metylpropen tác dụng với nước có xúc tác axit.
d. Trùng hợp but-1-en.
Lời giải:
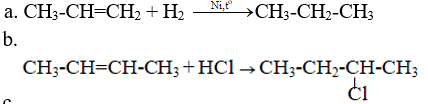
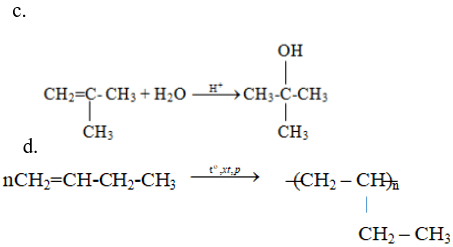
Giải bài 4 trang 132 Hóa 11 SGK
Trình bày phương pháp hóa học để :
a. Phân biệt metan và etilen.
b. Tách lấy khí metan từ hỗn hợp etilen.
c. Phân biệt hai bình không dán nhãn đựng hexan và hex-1-en.
Viết phương trình hoá học của phản ứng đã dùng.
Lời giải:
a. Lần lượt cho metan và etilen đi qua dung dịch nước brom, chất nào làm dung dịch nước brom nhạt màu thì đó là etilen, chất nào không làm dung dịch nước brom nhạt màu thì đó là metan.
CH2=CH2 + Br2 → CH2Br-CH2Br
Br2(dd nâu đỏ); CH2Br-CH2Br (không màu)
CH4 không tác dụng với dung dịch nước brom
b. Cho hỗn hợp khí (CH4 và C2H4) đi qua dung dịch nước brom dư, C2H4 sẽ tác dụng với dung dịch nước brom, khí còn lại ra khỏi bình dung dịch nước brom là CH4.(PTHH như câu a)
c. Tương tự câu a
Lần lượt cho hexan và hex-1-en đi qua dung dịch nước brom, chất nào làm dung dịch nước brom nhạt màu thì đó là hex-1-en, chất nào không làm dung dịch nước brom nhạt màu thì đó là hexan
PTHH:
CH2=CH-[CH2]3-CH3 + Br2 → CH2Br-CHBr-[CH2]3-CH3
Br2(dd nâu đỏ); CH2Br-CHBr-[CH2]3-CH3 (không màu)
Hexan không tác dụng với dung dịch nước brom
Giải bài 5 Hóa 11 SGK trang 132
Chất nào sau đây làm mất màu dung dịch brom?
A. Butan
B. but-1-en
C. cacbon đioxi
D. metylpropan
Lời giải:
Đáp án B
PTHH:
CH2=CH-CH2-CH3 + Br2 → CH2Br-CHBr-CH2-CH3
Br2(dd nâu đỏ); CH2Br-CHBr-CH2-CH3(không màu)
Giải bài 6 Hóa lớp 11 SGK trang 132
Dẫn từ từ 3,36 lít hỗn hợp gồm etilen và propilen (đktc) vào dung dịch brom thấy dung dịch bị nhạt màu và không có khí thoát ra. Khối lượng dung dịch sau phản ứng tăng 4,90gam.
a. Viết các phương trình hóa học và giải thích các hiện tượng ở thí nghiệm trên.
b. Tính thành phần phần trăm về thể tích của mỗi khí trong hỗn hợp ban đầu.
Lời giải:
a. Phương trình hóa học:
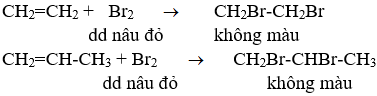
b. Gọi số mol của etilen và propilen lần lượt là x và y mol.
Khối lượng dung dịch sau phản ứng tăng lên chính là khối lượng của hỗn hợp etilen và propilen.
Ta có hệ phương trình:
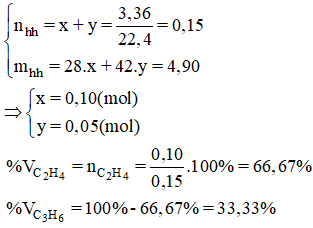
Lý thuyết Hóa 11 Bài 29: Anken
I. Đồng đẳng, cấu tạo
- Công thức chung: CnH2n (n ≥ 2).
- Tên gọi chung là anken hay olefin.
- Công thức đơn giản nhất là etilen (CH2=CH2).
- Mạch cacbon hở, có thể phân nhánh hoặc không phân nhánh.
- Trong phân tử có 1 liên kết đôi: gồm 1 liên kết σ và 1 liên kết π. Nguyên tử cacbon ở liên kết đôi tham gia 3 liên kết σ nhờ obitan lai hóa sp2, còn liên kết π nhờ obitan p không lai hóa.
- Đặc biệt phân tử CH2=CH2 có cấu trúc phẳng.
- Do có liên kết pi nên khoảng cách giữa hai nguyên tử C=C ngắn lại và nguyên tử cacbon này không thể quay quanh liên kết đôi vì khi quay như vậy liên kết π bị phá vỡ.
II. Đồng phân, danh pháp
1. Danh pháp
* Tên thông thường: Tên ankan – an + ilen
Ví dụ: CH2=CH2: etilen; CH2=CH–CH3: Propilen
* Tên thay thế: gọi tên theo cách sau:
- Chọn mạch chính là mạch C dài nhất có chứa liên kết đôi.
- Đánh số C mạch chính từ phía gần liên kết đôi hơn.
Gọi tên: vị trí nhánh – tên nhánh – tên C mạch chính – vị trí liên kết đôi – en.
CH2=CH-CH2-CH3: But–1–en.
CH3-CH=CH-CH3: But–2–en.
2. Đồng phân
a. Đồng phân cấu tạo
- Đồng phân vị trí liên kết đôi:
CH2=CH-CH2-CH3
CH3-CH=CH-CH3
- Đồng phân mạch cacbon:
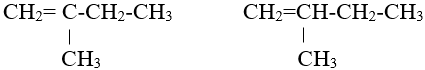
b. Đồng phân hình học
Ví dụ: But-2-en
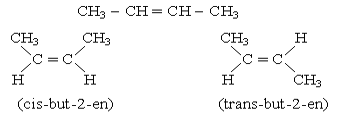
III. Tính chất vật lý
1. Nhiệt độ sôi, nhiệt độ nóng chảy và khối lượng riêng
- Nhiệt độ nóng chảy nhiệt độ sôi tăng dần khi tăng số nguyên tử cacbon trong phân tử: 4 chất đầu là chất khí, các chất có n từ 5 → 18 là chất lỏng, khi n≥19 là chất rắn.
- Các anken đều nhẹ hơn nước.
- Khối lượng riêng của anken không khác nhiều so với ankan và xicloankan có cùng số nguyên tử C.
2. Tính tan và màu sắc
- Đều ít tan trong nước, tan được trong một số dung môi nhưng dễ tan trong các dung môi hữu cơ (rượu, ete, …).
- Các anken không màu.
IV. Tính chất hóa học
1. Phản ứng cộng hiđro (Phản ứng hiđro hoá)
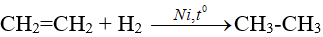
2. Phản ứng cộng halogen (Phản ứng halogen hoá)
CH2=CH2 + Br2 → Br–CH2–CH2–Br
- Anken làm mất màu của dung dịch brom → Phản ứng này dùng để nhận biết anken.
3. Phản ứng cộng nước và axit
- Cộng axit HX.
CH2=CH2 + HCl → CH3CH2Cl
- Đối với các anken khác, nguyên tử halogen (trong HX) mang điện âm, ưu tiên đính vào nguyên tử C bậc cao (theo quy tắc Maccopnhicop).
* Quy tắc Maccopnhicop: Trong phản ứng cộng HX (axit hoặc nước) vào liên kết C=C của anken, H (phần mang điện tích dương) cộng vào C mang nhiều H hơn, X- (hay phần mang điện tích âm) cộng vào C mang ít H hơn.
- Cộng nước:
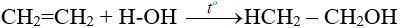
4. Phản ứng trùng hợp
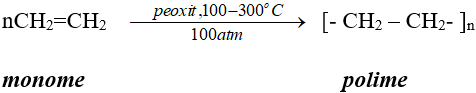
- Phản ứng trùng hợp là quá trình cộng hợp liên tiếp nhiều phân tử nhỏ giống nhau hoặc tương tự nhau tạo thành phân tử lớn gọi là polime.
- Số lượng mắt xích trong một phân tử polime gọi là hệ số trùng hợp, kí hiệu n.
5. Phản ứng oxi hoá
- Oxi hoá hoàn toàn:
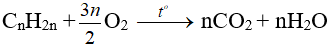
Nhận xét: Đốt anken thu nCO2 = nH2O
- Oxi hoá không hoàn toàn:
3CH2=CH2 + 4H2O + 2KMnO4 → 3HO–CH2–CH2–OH + 2MnO2↓ + 2KOH
Anken làm mất màu dd KMnO4 → Dùng để nhận biết anken.
V. Điều chế và ứng dụng
1. Điều chế
Trong phòng thí nghiệm:
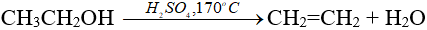
Trong công nghiệp:
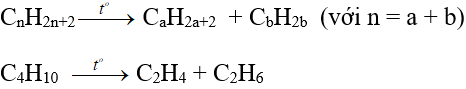
2. Ứng dụng
a. Tổng hợp polime
- Trùng hợp etilen, propilen, butilen người ta thu được các polime để chế tạo màng mỏng, bình chứa, ống dẫn nước, ... dùng cho nhiều mục đích khác nhau.
- Chuyển hoá etilen thành các monome khác để tổng hợp ra hàng loạt polime đáp ứng nhu cầu phong phú của đời sống và kĩ thuật.
Ví dụ:
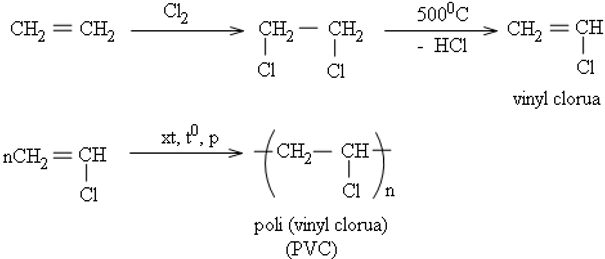
b. Tổng hợp các hoá chất khác
Từ etilen tổng hợp ra những hoá chất hữu cơ thiết yếu như etanol, etilen oxit, etylen glicol, anđehit axetic, ...
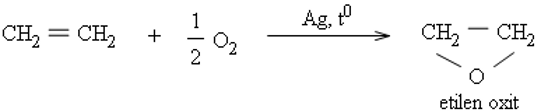
►►CLICK NGAY vào nút TẢI VỀ dưới đây để tải về Giải Hoá học 11 Bài 29: Anken trang 132 SGK file PDF hoàn toàn miễn phí!
 Giải Hoá học 11 Bài 31: Luyện tập : Anken và ankađien trang 137, 138 SGK
Giải Hoá học 11 Bài 31: Luyện tập : Anken và ankađien trang 137, 138 SGK Giải Hoá học 11 Bài 34: Bài thực hành 4 SGK
Giải Hoá học 11 Bài 34: Bài thực hành 4 SGK Giải Hoá học 11 Bài 33: Luyện tập : Anken trang 147 SGK
Giải Hoá học 11 Bài 33: Luyện tập : Anken trang 147 SGK Giải Hoá học 11 Bài 32: Ankin trang 145 SGK
Giải Hoá học 11 Bài 32: Ankin trang 145 SGK Giải Hoá học 11 Bài 30: Ankađien trang 135, 136 SGK
Giải Hoá học 11 Bài 30: Ankađien trang 135, 136 SGK Giải Hoá học 11 Bài 29: Anken trang 132 SGK
Giải Hoá học 11 Bài 29: Anken trang 132 SGK

