Giải SBT Hóa học 12 Bài 37: Luyện tập: Tính chất hóa học của sắt và hợp chất của sắt (chính xác nhất)
Mời các em học sinh và quý thầy cô tham khảo ngay hướng dẫn giải Giải SBT Hóa học 12 Bài 37: Luyện tập: Tính chất hóa học của sắt và hợp chất của sắt (Chính xác nhất) được đội ngũ chuyên gia biên soạn ngắn gọn và đầy đủ dưới đây.
Giải Hóa học 12 Bài 37 SBT: Luyện tập: Tính chất hóa học của sắt và hợp chất của sắt
Bài 37.1 trang 90 Sách bài tập Hóa học 12:
Để bảo quản dung dịch FeSO4 trong phòng thí nghiêm, người ta ngâm vào dung dịch đó một đinh sắt đã làm sạch. Chọn cách giải thích đúng cho việc làm trên.
A. Để Fe tác dụng hết với H2SƠ4 dư khi điều chế FeSO4 bằng phản ứng :
Fe + H2SO4(loãng) → FeSO4 + H2↑
B. Để Fe tác dụng với các tạp chất trong dung dịch, chẳng hạn với tạp chất là CuSO4 :
Fe + CuSO4 → FeSO4 + Cu
C. Để sắt tác dụng hết O2 hoà tan :
2Fe + O2 → 2FeO
D. Để sắt khử muối sắt(III) thành muối sắt(II) :
Fe + Fe2(SO4)3 → 3FeSO4
Lời giải:
D
Bài 37.2 trang 90 Sách bài tập Hóa học 12:
Cho hai phương trình hoá học sau :
Cu + 2FeCl3 → 2FeCl2 + CuCl2 Fe + CuCl2 → FeCl2 + Cu
Có thể rút ra kết luận nào sau đây
A. Tính oxi hoá : Fe3+ > Cu2+ > Fe2+.
B. Tính oxi hoá : Fe2+ > Cu2+ > Fe3+.
C. Tính khử : Fe > Fe2+ > Cu.
D. Tính khử : Fe2+ > Fe > Cu.
Lời giải:
A
Bài 37.3 trang 90 Sách bài tập Hóa học 12:
Nhúng thanh sắt (đã đánh sạch) vào các dung dịch ở ba thí nghiệm sau :
Thí nghiệm 1 : nhúng vào dung dịch CuSO4.
Thí nghiệm 2 :- nhúng vào dung dịch NaOH.
Thí nghiệm 3 : nhúng vào dung dịch Fe2(SO4)3.
Giả sử rằng các kim loại sinh ra (nếu có) đều bám vào thanh sắt thì nhận xét nào sau đây đúng ?
A. Ở thí nghiệm 1, khối lượng thanh sắt giảm.
B. Ở thí nghiệm 2, khối lượng thanh sắt không đổi.
C. Ớ thí nghiệm 3, khối lượng thanh sắt không đổi.
D. A, B, C đều đúng.
Lời giải:
B
Bài 37.4 trang 91 Sách bài tập Hóa học 12:
Cho khí CO khử hoàn toàn 10 g quặng hematit. Lượng sắt thu được cho tác dụng hết với dung dịch H2SO4 loãng thu được 2,24 lít H2 (đktc). Phần trăm khối lượng của Fe2O3 trong quặng là
A. 70%.
B. 75%.
C. 80%.
D. 85%.
Lời giải:
C
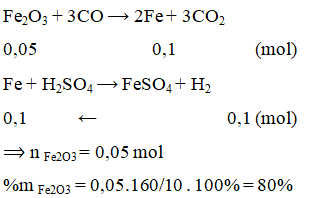
Bài 37.5 trang 91 Sách bài tập Hóa học 12:
Cho 6,72 gam Fe vào dung dịch chứa 0,3 mol H2SO4 đặc, nóng (giả thiết SO2 là sản phẩm khử duy nhất). Sau khi phản ứng xảy ra hoàn toàn, thu được
A. 0,03 mol Fe2(SO4)3 và 0,06 mol FeSO4
B. 0,05 mol Fe2(SO4)3 0,02 mol Fe dư.
C. 0,02 mol Fe2(SO4)3 và 0,08 mol FeSO4.
D. 0,12 mol FeSO4.
Lời giải:
A
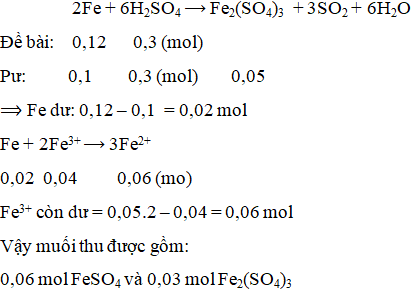
Bài 37.6 trang 91 Sách bài tập Hóa học 12:
Cho khí CO khử hoàn toàn đến Fe một hỗn hợp gồm : FeO, Fe2O3, Fe3O4 thấy có 4,48 lít CO2 (đktc) thoát ra. Thể tích CO (đktc) đã tham gia phản ứng là
A. 1,12 lít.
B. 2,24 lít.
C. 3,36 lít.
D. 4,48 lít.
Lời giải:
D
CO + [O] ⟶ CO2
VCO = VCO2 = 4,48 lít
Bài 37.7 trang 91 Sách bài tập Hóa học 12:
Cho 11,36g hỗn hợp gồm Fe, FeO, Fe2O3 và Fe3O4 phản ứng hết với dung dịch HNO3 loãng dư, thu được 1,344 lít khí NO (sản phẩm khử duy nhất, ở đktc) và dung dịch X. Cô cạn dung dịch X thu được m g muối khan. Giá trị m là
A. 43,076
B. 34,076
C. 43,706
D. 34,706
Lời giải:
A
Quy đổi hỗn hợp thành: FeO (x mol) và O2 (y mol)
Ta có: 72x + 32y = 11,36g
Bảo toàn e ta có: nFeO = 4nO2 + 3nNO ⟹ x – 4y = 0,18 mol
⟹ x = 0,16 mol; y = - 0,005mol
Bảo toàn nguyên tố Fe: nFe(NO3)3 = nFeO = 0,16 mol
⟹ mmuối = 0,16.242 = 38,72g
Bài 37.8 trang 92 Sách bài tập Hóa học 12:
Thực hiện những biến đổi hoá học trong sơ đồ sau bằng cách viết phương trình hoá học của các phản ứng và nêu điều kiện của phản ứng (nếu có).
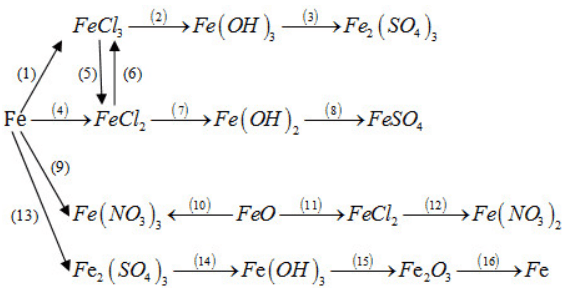
Lời giải:
(1) 2Fe + 3Cl2 to→ 2FeCl3
(2) FeCl3 + 3NaOH → Fe(OH)3 + 3NaCl
(3) 2Fe(OH)3 + 3H2SO4 → Fe2(SO4)3 + 3H2O
(4) Fe + 2HCl → FeCl2 + H2
(5) 2FeCl3 + Fe → 3FeCl2
(6) 2FeCl2 + Cl2 → 2FeCl3
(7) FeCl2 + 2NaOH → Fe(OH)2 + 2NaCl
(8) Fe(OH)2 + H2SO4 → FeSO4 + 2H2O
(9) Fe + 4HNO3 → Fe(NO3)3 + NO + 2H2O
(10) FeO + 4HNO3 → Fe(NO3)3 + NO2 + 2H2O
(11) FeO + 2HCl → FeCl2 + H2O
(12) FeCl2 + 2AgNO3→ Fe(NO3)2 + 2AgCl↓
(13) 2Fe + 6H2SO4 (đ) → Fe2(SO4)3 + 3SO2 +6H2O
(14) Fe2(SO4)3 + 6NaOH → 2Fe(OH)3↓ + 3Na2SO4
(15) 2Fe(OH)3 to→ Fe2O3 + 3H2O
(16) Fe2O3 + 3CO to→ 2Fe + 3CO2
Bài 37.9 trang 92 Sách bài tập Hóa học 12:
Dung dịch A có chứa CuSO4 và Fe2(SO4)3
a) Thêm Mg vào dung dịch A → dung dịch B có 3 muối tan.
b) Thêm Mg vào dung dịch A → dung dịch C có 2 muối tan.
Viết PTHH của các phản ứng xảy ra.
Lời giải:
a) Mg +Fe2(SO4)3 → MgSO4 + 2FeSO4 (1)
Mg + CuSO4 → MgS04 + Cu (2)
Dung dịch B có 3 muối là MgSO4, FeSO4 và CuSO4 dư.
b) Dung dịch C có 2 muối tan là MgSO4 và FeSO4.
Bài 37.10 trang 92 Sách bài tập Hóa học 12:
Muốn có đủ khí clo để tác dụng với 1,12 g Fe cần phải dùng bao nhiêu gam K2Cr2O7 và bao nhiêu mililít dung dịch HCl 36,5% (D = 1,19 g/ml)
Lời giải:
nFe = 1,12: 56= 0,04 mol
Các phản ứng xảy ra:
K2Cr2O7 + 14HCl → 2KCl + 2CrCl3 + 3Cl2 + 7H2O (1)
2Fe + 3Cl2 → 2FeCl3 (2)
Theo pt (2) ta có : nCl2 = 3/2nFe = 0,03 mol
Theo pt (1) ta có :
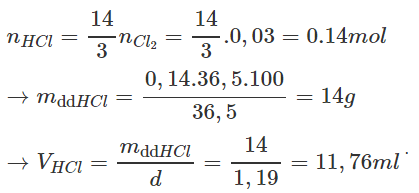
nK2Cr2O7 = nCl2/3 = 0,01 mol
mK2Cr2O7 = 0,01 x 294 = 2,94g
Bài 37.11 trang 92 Sách bài tập Hóa học 12:
Hỗn hợp A gồm Fe và kim loại M có hoá trị không đổi trong mọi hợp chất, M đứng trước hiđro trong dãy điện hoá. Tỉ lệ số mol của M và Fe trong hỗn hợp A là 1 : 2. Cho 13,9 g hỗn hợp A tác dụng với khí Cl2 thì cần dùng 10,08 lít Cl2. Cho 13,9 g hỗn hợp A tác dụng với dung dịch HCl thì thu được 7,84 lít H2. Các thể tích khí đều đo ở đktc. Xác định kim loại M và % khối lượng của mỗi kim loại trong hỗn hợp A.
Lời giải:
2M + 2nHCl → MCln + n H2
x 0,5nx(mol)
Fe + 2HCl → FeCl2 + H2
2x 2x (mol)
0,5nx + 2x = 7,84/22,4 = 0,35 (1)
2M + nCl2 → 2MCln
x 0,5nx(mol)
2Fe + 3Cl2 → 2FeCl3
2x 3x (mol)
0,5nx + 3x = 10,08/22,4 = 0,45 (2)
Từ (1) và (2) → n= 3, x= 0,1
mFe = 2.0,1.56= 11,2 g ; m M = 13,9-11,2= 2,7g
→ M M = 2,7:0,1 = 27 → M là Al
%mAl = 2,7/13,9 x 100% = 19,42%
%mFe = 80,58%
Bài 37.12 trang 92 Sách bài tập Hóa học 12:
Cho luồng khí co dư đi qua ống sứ đựng m gam hỗn hợp FeO và Fe2O3 nung nóng. Sau khi kết thúc phản ứng, khối lượng chất rắn trong ống sứ là 5,5 gam. Cho khí đi ra khỏi ống sứ hấp thụ vào nước vôi trong dư thấy có 5 gam kết tủa. Xác định giá trị của m.
Lời giải:
Ta có sơ đồ phản ứng :
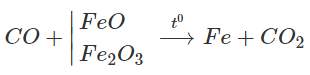
Nhận thấy, cứ 1 mol CO phản ứng sinh ra 1 mol CO2 thì khối lượng chất rắn giảm 16 gam
Mặt khác ta có : n CO2 = nCaCO3 = 0,05 mol ⟹ khối lượng rắn giảm = 0,05.16 = 0,8 (gam)
⟹ Khối lượng hỗn hợp oxit ban đầu là: m = 5,5 + 0,8 = 6,3g
Bài 37.13 trang 92 Sách bài tập Hóa học 12:
Cho 18,5 gam hỗn hợp X gồm Fe, Fe3O4 tác dụng với 200 ml dung dịch HNO3 loãng đun nóng và khuấy đều. Sau khi phản ứng xảy ra hoàn toàn được 2,24 lít khí NO duy nhất (đktc), dung dịch Y và còn lại 1,46 gam kim loại. Xác định khối lượng muối trong Y và nồng độ mol của dung dịch HNO3.
Lời giải:
Sau phản ứng kim loại còn dư, vậy Fe chỉ bị oxi hoá lên Fe2+
Gọi x, y là số mol Fe và Fe3O4 phản ứng, khối lượng rắn phản ứng là
18,5- 1,46 = 17,04 (gam).
⟹ 56x + 232y = 17,04 gam (1)
Ta có phương trình cho - nhận e :
Fe → Fe2+ + 2e
x → x → 2x mol
Fe3O4 + 2e → 3Fe+2
y → 2y → 3y (mol)
N+5 + 3e → N+2
0,3 ← 0,1 (mol)
Áp dụng ĐLBTĐT, ta có : 2x = 2y + 0,3 (2)
Từ (1) và (2), giải hệ ta có : x = 0,18; y = 0,03
Vậy muối thu được là Fe(NO3)2 : (x + 3y) = 0,27 mol ⟹ m = 48,6 g
Số mol HNO3 phản ứng = 2.nFe(NO3)2 +nN0 = 2.0,27 + 0,1 = 0,64 mol
⟹ CM(HNO3) = 3,2 (M).
Bài 37.14 trang 93 Sách bài tập Hóa học 12:
Hoà tan hoàn toàn 10 gam hỗn hợp X (Fe, Fe2O3) trong dung dịch HNO3 vừa đủ được 1,12 lít NO (đktc, sản phẩm khử duy nhất) và dung dịch Y. Cho Y tác dụng với NaOH dư được kết tủa Z. Nung Z trong không khí đến khối lượng không đổi được m gam chất rắn. Xác định giá trị của m.
Lời giải:
Ta có sơ đồ phản ứng:
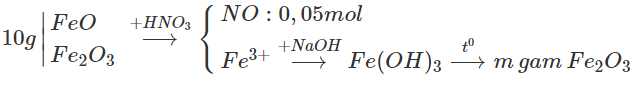
Vì chỉ có Fe phản ứng sinh ra khí NO, sử dụng phương trình cho - nhận e
⟹ nFe = nNO = 0,05 mol.
m Fe ban đầu = 0,05.56 = 2,8(gam) ⟹ m Fe2O3 sau = 160.0,025 = 4(gam)
m Fe2O3 ban đầu = 10 - 2,8 = 7,2 g
Vậy m = 4 + 7,2 =11,2 (gam).
►►CLICK NGAY vào nút TẢI VỀ dưới đây để tải về Giải SBT Hóa 12 Bài 37: Luyện tập: Tính chất hóa học của sắt và hợp chất của sắt (Ngắn gọn nhất) file PDF hoàn toàn miễn phí.
 Giải SBT Hóa học 12 Bài 33: Hợp kim của sắt (chính xác nhất)
Giải SBT Hóa học 12 Bài 33: Hợp kim của sắt (chính xác nhất) Giải SBT Hóa học 12 Bài 7: Luyện tập: Cấu tạo và tính chất của cacbohiđrat (chính xác nhất)
Giải SBT Hóa học 12 Bài 7: Luyện tập: Cấu tạo và tính chất của cacbohiđrat (chính xác nhất) Giải SBT Hóa học 12 Bài 18: Tính chất của kim loại. Dãy điện hóa của kim loại (chính xác nhất)
Giải SBT Hóa học 12 Bài 18: Tính chất của kim loại. Dãy điện hóa của kim loại (chính xác nhất) Giải SBT Hóa học 12 Bài 13: Đại cương về polime (chính xác nhất)
Giải SBT Hóa học 12 Bài 13: Đại cương về polime (chính xác nhất) Giải SBT Hóa học 12 Bài 1: Este (chính xác nhất)
Giải SBT Hóa học 12 Bài 1: Este (chính xác nhất) Giải SBT Hóa học 12 Bài 6: Saccarozơ, tinh bột và xenlulozơ (chính xác nhất)
Giải SBT Hóa học 12 Bài 6: Saccarozơ, tinh bột và xenlulozơ (chính xác nhất) Giải SBT Hóa học 12 Bài 5: Glucozơ (chính xác nhất)
Giải SBT Hóa học 12 Bài 5: Glucozơ (chính xác nhất) Giải SBT Hóa học 12 Bài 34: Crom và hợp chất của crom (chính xác nhất)
Giải SBT Hóa học 12 Bài 34: Crom và hợp chất của crom (chính xác nhất)

